题目内容
 氢的存储是氢能应用的主要瓶颈,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等.
氢的存储是氢能应用的主要瓶颈,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等.(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料.
①Ti的基态原子有
②BH-4的空间构型是
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2?2NH3实现储氢和输氢.下列说法正确的是
A.NH3分子中N原子采用sp3杂化
B.NH3分子的空间构型是正四面体
C.NH3和NH4+是等电子体
D.CN-的电子式为:
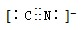
E.相同压强时,NH3沸点比PH3高
(3)2008年,Yoon等人发现Ca与C60生成的Ca32C60能大量吸附H2分子.
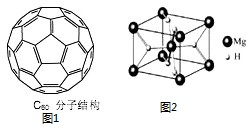
①C60晶体易溶于苯、CS2,说明C60是
②C60分子结构如图1所示,则C60分子中含有π键数目为
(4)MgH2是金属氢化物储氢材料,其晶胞结构如图2所示.
①MgH2遇水就能释放H2,该反应的化学方程式为
②已知该晶体的密度a g?cm-3,则该晶胞的体积为
考点:晶胞的计算,原子核外电子排布,原子轨道杂化方式及杂化类型判断,不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:(1)①钛是22号元素,根据构造原理书写其基态核外电子排布式,确定不同能量的电子的各类;
②根据价层电子对互斥理论确定空间构型;
(2)A.根据价层电子对互斥理论确定杂化方式;
B.根据中心原子的杂化方式及孤电子对数可以判断NH3分子的空间构型;
C.根据等电子体的概念,互为等电子体的两个微粒要价电子数相等,据此判断;
D.CN-与氮气互为等电子体,结构与氮气相同,据此可以判断CN-的电子式为: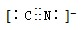
E.由于氨分子之间有氢键,所以相同压强时,NH3沸点比PH3高,据此判断;
(3)①根据相似相溶原理确定分子的极性;
②利用均摊法计算;
(4)①根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
②利用均摊法计算该晶胞中镁、氢原子个数,再根据V=
进行计算.
②根据价层电子对互斥理论确定空间构型;
(2)A.根据价层电子对互斥理论确定杂化方式;
B.根据中心原子的杂化方式及孤电子对数可以判断NH3分子的空间构型;
C.根据等电子体的概念,互为等电子体的两个微粒要价电子数相等,据此判断;
D.CN-与氮气互为等电子体,结构与氮气相同,据此可以判断CN-的电子式为:
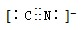
E.由于氨分子之间有氢键,所以相同压强时,NH3沸点比PH3高,据此判断;
(3)①根据相似相溶原理确定分子的极性;
②利用均摊法计算;
(4)①根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
②利用均摊法计算该晶胞中镁、氢原子个数,再根据V=
| m |
| ρ |
解答:
解:(1)①钛是22号元素,根据构造原理知其基态核外电子排布式为:1s22s22p63s23p63d24s2,所以有7种不同能量的电子,故答案为:7;
②BH4-中B原子价层电子对=4+
(3+1-4×1)=4,且没有孤电子对,所以是正四面体结构,故答案为:正四面体;
(2)A.NH3分子中N原子含有3个共用电子对和一个孤电子对,所以其价层电子对是4,采用sp3杂化,故正确;
B.根据中心原子的杂化方式为sp3杂化且有一对孤电子对数可以判断NH3分子的空间构型为三角锥形,故错误;
C.根据等电子体的概念,互为等电子体的两个微粒要价电子数相等,而NH3和NH4+价电子数不等,故错误;
D.CN-与氮气互为等电子体,结构与氮气相同,据此可以判断CN-的电子式为: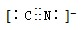 ,故正确;
,故正确;
E.由于氨分子之间有氢键,所以相同压强时,NH3沸点比PH3高,故正确;
故答案为:ADE;
(3)①苯、CS2都是非极性分子,根据相似相溶原理知,C60是非极性分子,故答案为:非极性;
②利用均摊法知,每个碳原子含有
个π 键,所以1mol C60分子中,含有π键数目=
×1mol×60×NA/mol=30NA,故答案为:30NA;
(4)①氢化镁固体与水反应的化学方程式为:MgH2+2H2O═Mg(OH)2+2H2↑,故答案为:MgH2+2H2O═Mg(OH)2+2H2↑;
②该晶胞中镁原子个数=
×8+1=2,氢原子个数=2+4×
,V=
=
cm3=
cm3,故答案为:
.
②BH4-中B原子价层电子对=4+
| 1 |
| 2 |
(2)A.NH3分子中N原子含有3个共用电子对和一个孤电子对,所以其价层电子对是4,采用sp3杂化,故正确;
B.根据中心原子的杂化方式为sp3杂化且有一对孤电子对数可以判断NH3分子的空间构型为三角锥形,故错误;
C.根据等电子体的概念,互为等电子体的两个微粒要价电子数相等,而NH3和NH4+价电子数不等,故错误;
D.CN-与氮气互为等电子体,结构与氮气相同,据此可以判断CN-的电子式为:
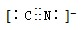 ,故正确;
,故正确;E.由于氨分子之间有氢键,所以相同压强时,NH3沸点比PH3高,故正确;
故答案为:ADE;
(3)①苯、CS2都是非极性分子,根据相似相溶原理知,C60是非极性分子,故答案为:非极性;
②利用均摊法知,每个碳原子含有
| 1 |
| 2 |
| 1 |
| 2 |
(4)①氢化镁固体与水反应的化学方程式为:MgH2+2H2O═Mg(OH)2+2H2↑,故答案为:MgH2+2H2O═Mg(OH)2+2H2↑;
②该晶胞中镁原子个数=
| 1 |
| 8 |
| 1 |
| 2 |
| m |
| ρ |
| ||
| a |
| 52 |
| a?NA |
| 52 |
| a?NA |
点评:本题考查物质结构和性质,涉及核外电子排布、杂化方式的判断、空间构型的判断、晶胞的计算等知识点,难点是晶胞的计算,灵活运用公式是解本题关键,难度中等.

练习册系列答案
相关题目
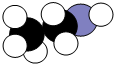 如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子.关于该物质说法不正确为( )
如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子.关于该物质说法不正确为( )| A、不能使紫色石蕊变红 |
| B、与碳酸钠反应 |
| C、能发生酯化反应 |
| D、能发生氧化反应催化剂 |
下列实验操作或装置错误的是( )
A、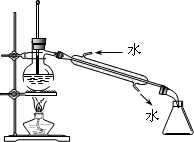 蒸馏 |
B、 过滤 |
C、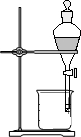 萃取 |
D、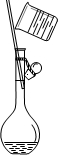 转移溶液 |
下列每组中各有两对物质,它们都能用分液漏斗分离的是( )
| A、溴苯和水,酒精和水 |
| B、四氯化碳和水,溴苯和己烷 |
| C、豆油和水,苯和溴苯 |
| D、汽油和水,己烷和水 |
下列物质中,只含有离子键的化合物是( )
| A、KOH |
| B、NH4Cl |
| C、HCl |
| D、MgCl2 |
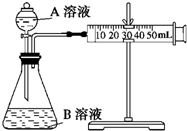 甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.