题目内容
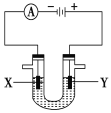
【题目】如图所示,四支电极均为铂电极,供选择的四组电解质溶液如下表:
组 | A | B | C | D |
甲槽 | NaOH溶液 | AgNO3溶液 | H2SO4溶液 | NaCl溶液 |
乙槽 | CuSO4溶液 | CuCl2溶液 | AgNO3溶液 | AgNO3溶液 |
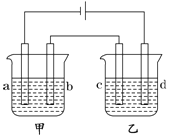
要满足的条件是:①工作一段时间后,甲槽电解液pH上升,而乙槽电解液pH下降;②b、c两极放电离子的物质的量相等。则:
(1)应选用的电解液是________组。
(2)甲槽的电解方程式为:_____________;乙槽的电解方程式为:_______________。
【答案】D 2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑ 4AgNO3+2H2O
2NaOH+Cl2↑+H2↑ 4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3
4Ag+O2↑+4HNO3
【解析】
①工作一段时间后甲槽pH上升,乙槽的pH下降。②b、c两极上反应的离子的物质的量相等。惰性电极电解;
A组、甲槽是电解水,氢氧化钠溶液pH增大,b电极是阳极,电极反应为:4OH--4e-=2H2O+O2↑;乙槽电解硫酸铜溶液,溶液pH减小,c电极为阴极,电解反应为:Cu2++2e-=Cu,依据电子守恒可知,b、c两极上反应的离子的物质的量不相等:
B组、甲槽是电解硝酸银,溶液pH减小,b电极是阳极,电极反应为:4OH--4e-=2H2O+O2↑;乙槽电解氯化铜溶液,溶液pH减小,c电极为阴极,电解反应为:Cu2++2e-=Cu,依据电子守恒可知,b、c两极上反应的离子的物质的量不相等:
C组、甲槽是电解水,硫酸溶液pH变小,b电极是阳极,电极反应为:4OH--4e-=2H2O+O2↑;乙槽电解硝酸银溶液,溶液pH减小,c电极为阴极,电解反应为:4Ag++4e-=4Ag,依据电子守恒可知,b、c两极上反应的离子的物质的量相等:
D组、甲槽是电解氯化钠,氯化钠溶液pH增大,b电极是阳极,电极反应为:4OH--4e-=2H2O+O2↑;乙槽电解硝酸银溶液,溶液pH减小,c电极为阴极,电解反应为:4Ag++4e-=4Ag,依据电子守恒可知,b、c两极上反应的离子的物质的量相等;
依据电极反应和电极过程中溶液pH变化分析判断。
(1)依据上述分析可知,符合条件的是D组;
(2)甲槽电解食盐水生成氢氧化钠、氯气和氢气,甲槽的电解方程式为:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑;乙槽电解硝酸银溶液生成银、氧气和硝酸,乙槽的电解方程式为:4AgNO3+2H2O
2NaOH+Cl2↑+H2↑;乙槽电解硝酸银溶液生成银、氧气和硝酸,乙槽的电解方程式为:4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3。
4Ag+O2↑+4HNO3。