题目内容
【题目】如图所示为密闭容器中反应C+H2O(g)![]() CO+H2 ΔH>0达到平衡后,由于条件改变而引起正、逆反应速率的变化以及平衡移动的情况。下列说法错误的是
CO+H2 ΔH>0达到平衡后,由于条件改变而引起正、逆反应速率的变化以及平衡移动的情况。下列说法错误的是
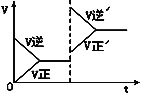
A. 起始反应物为CO和H2
B. 改变条件后平衡逆向移动
C. 改变的条件是增大压强
D. 新平衡时CO的浓度比原平衡小
【答案】D
【解析】A. 根据图像,起始时,逆反应速率大于正反应速率,且正反应速率为0,说明起始反应物为CO和H2,故A正确;B.根据图像, 改变条件后,逆反应速率大于正反应速率,平衡逆向移动,故B正确;C. 改变的条件后,逆反应速率和正反应速率均增大,且逆反应速率大于正反应速率,增大压强,平衡逆向移动,逆反应速率大于正反应速率,与图像吻合,故C正确;D.根据C的分析,改变的条件是增大压强,体积减小,新平衡时CO的浓度比原平衡大,故D错误;故选D。

练习册系列答案
相关题目
【题目】(1)H3PO2是一元中强酸,写出其电离方程式_______________________________。NaH2PO2为__________(填“正盐”或“酸式盐”),其溶液显__________(填“弱酸性”、“中性”或“弱碱性”)
(2)下表列出了某冷轧厂排放的废水中各成分的含量及国家环保标准值的有关数据:
冷轧含锌废水水质 | 经处理后的水国家环保标准值 | |
Zn2+浓度/(mg·L-1) | ≤800 | ≤3.9 |
pH | 1~5 | 6~9 |
SO42-浓度/(mg·L-1) | ≤23000 | ≤150 |
经某一工艺处理后的废水pH=8,常温下,该废水中Zn2+的浓度为__________mg·L-1(常温下,Ksp[Zn(OH)2]=1.2×10-17),__________(填“符合”或“不符合”)国家环保标准。