题目内容
【题目】已知某市售“84消毒液”瓶体部分标签如下图所示,该“84 消毒液”通常稀释100 倍(体积之比)后使用.请回答下列问题:

(1)该“84 消毒液”的物质的量浓度约为__mol/L.( 保留小数点后 1 位)
(2)该同学参阅此“84 消毒液”的配方,欲用NaClO固体配制480mL 与市售物质的量浓度相同的“84 消毒液”,下列说法中正确的是__( 填序号).
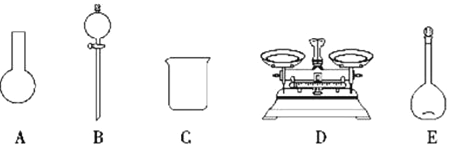
A.如下图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0g
(3)“84 消毒液”与稀硫酸混合使用可增强其消毒能力,某消毒小组人员用 98%( 密度为1.84g/cm3)的浓硫酸配制 500mL 2.3mol/L 的稀硫酸用于增强“84 消毒液”的消毒能力.
①需用浓硫酸的体积为__mL.
②取用任意体积的浓硫酸时,下列物理量中不随所取体积的多少而变化的是__。
A.溶液中H2SO4的物质的量 B.溶液的浓度
C.溶液的质量 D.溶液的密度
③对浓硫酸稀释过程中遇到下列情况,使所配制的硫酸浓度大于2.3mol/L有__。
A.未经冷却趁热将溶液注入容量瓶中
B.摇匀后发现液面低于刻度线,再加水至刻度线
C.容量瓶中原有少量蒸馏水
D.定容时俯视观察液面.
【答案】 4.0 C 62.5 BD AD
【解析】试题(1)c(NaClO)=c=![]() =
=![]() =4.0molL-1,故答案为:4.0;
=4.0molL-1,故答案为:4.0;
(2)A.需用托盘天平称量NaClO固体,需用烧杯来溶解NaClO,需用玻璃棒进行搅拌和引流,需用容量瓶和胶头滴管来定容,图示的A、B、不需要,但还需玻璃棒和胶头滴管,故A错误;B.配制过程中需要加入水,所以经洗涤干净的容量瓶不必烘干后再使用,故B错误;C.由于NaClO易吸收空气中的H2O、CO2而变质,所以商品NaClO可能部分变质导致NaClO减少,配制的溶液中溶质的物质的量减小,结果偏低,故C正确;D.应选取500mL的容量瓶进行配制,然后取出480mL即可,所以需要NaClO的质量:0.5L×4.0molL-1×74.5gmol-1=149g,故D错误;故答案为:C;
(3)①溶液稀释前后溶质的物质的量不变,浓硫酸的浓度为c=![]() =18.4mol/L,假设需要浓硫酸的体积为V,则V×18.4mol/L=0.5L×2.3mol/L,V=0.625L=62.5mL,故答案为:62.5;
=18.4mol/L,假设需要浓硫酸的体积为V,则V×18.4mol/L=0.5L×2.3mol/L,V=0.625L=62.5mL,故答案为:62.5;
②A.溶液中H2SO4的物质的量n=cV,与体积有关,错误;B.溶液具有均一性,溶液的浓度与体积无关,正确;C.溶液的质量m=ρV,与体积有关,错误;D.溶液具有均一性,溶液的密度与体积无关,正确;故选BD;
③A.未经冷却趁热将溶液注入容量瓶中,导致溶液体积偏小,浓度偏大,正确;B.摇匀后发现液面低于刻度线,再加水至刻度线,导致溶液体积偏大,浓度偏小,错误;C.容量瓶中原有少量蒸馏水对结果无影响,错误;D.定容时俯视观察液面,导致溶液体积偏小,浓度偏大,正确;故选AD。

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案