题目内容
【题目】亚硝酸钙是一种阻锈剂,可用于染料工业,某兴趣小组拟制备Ca(NO2)2并对其性质进行探究。
(背景素材)
Ⅰ.NO+NO2+Ca(OH)2=Ca(NO2)2+H2O。
Ⅱ.Ca(NO2)2能被酸性KMnO4溶液氧化成NO3—,MnO4—被还原为Mn2+。
Ⅲ.在酸性条件下,Ca(NO2)2能将I氧化为I2,S2O32—能将I2还原为I。
(制备氮氧化物)
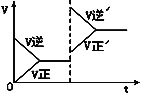
(1)甲组同学拟利用如下左图所示装置制备氮氧化物。

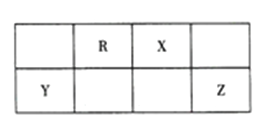
①仪器X、Y的名称分别是______________、______________。
②装置B中逸出的NO与NO2的物质的量之比为1∶1,则装置B中发生反应的化学方程式为______,若其他条件不变,增大硝酸的浓度,则会使逸出的气体中n(NO2)__________n(NO)(填“>”或“<”)。
(制备Ca(NO2)2)
(2)乙组同学拟利用装置B中产生的氮氧化物制备Ca(NO2)2,装置如上右图。
①装置C中导管末端接一玻璃球的作用是________________。
②装置D的作用是______________;装置E的作用是________________。
(测定Ca(NO2)2的纯度)
(3)丙组同学拟测定Ca(NO2)2的纯度(杂质不参加反应),可供选择的试剂:
a.稀硫酸 b.c1mol·L1的KI溶液 c.淀粉溶液 d.c2 mol·L1的Na2S2O3溶液 e.c3mol·L1的酸性KMnO4溶液
①利用Ca(NO2)2的还原性来测定其纯度,可选择的试剂是__________(填字母)。
②利用Ca(NO2)2的氧化性来测定其纯度的步骤:准确称取mgCa(NO2)2样品放入锥形瓶中,加适量水溶解,_______(请补充完整实验步骤)。
【答案】分液漏斗锥形瓶2SO2+2HNO3+H2O=NO+NO2+2H2SO4>增大与石灰乳的接触面积防止倒吸(或作安全瓶)吸收未反应的氮氧化物e加入过量c1 mol·L1的KI溶液、淀粉溶液,然后滴加稀硫酸,用c2 mol·L1的Na2S2O3溶液滴定至溶液由蓝色恰好变为无色,且半分钟内不变色,读取消耗Na2S2O3溶液的体积,重复以上操作2~3次
【解析】
(1) ①仪器X、Y分别是分液漏斗、锥形瓶,故答案为:分液漏斗、锥形瓶;
②根据题意,装置B中盛放的是硝酸,二氧化硫与硝酸反应放出一氧化氮和二氧化氮,若逸出的NO与NO2的物质的量之比为1∶1,则装置B中发生反应的化学方程式为2SO2+2HNO3+H2O=NO+NO2+2H2SO4,若其他条件不变,硝酸的浓度越大,生成的二氧化氮越多,则会使逸出的气体中n(NO2)>n(NO) ,故答案为:2SO2+2HNO3+H2O=NO+NO2+2H2SO4;>;
⑵①装置C中导管末端接一玻璃球,可以增大与石灰乳的接触面积,故答案为:增大与石灰乳的接触面积;
②反应中,装置内气体的压强会发生变化,装置D可以防止倒吸;装置E中的氢氧化钠可以吸收未反应的氦氧化物,防止污染空气,故答案为:防止倒吸(或作安全瓶) ;吸收未反应的氦氧化物,防止污染空气;
⑶ ①根据信息Ⅱ.Ca(NO2)2能被酸性KMnO4溶液氧化成NO3-,MnO4-被还原为Mn2+,利用Ca(NO2)2的还原性来测定其纯度,可选择的试剂是c3mol·L-1 的酸性 KMnO4 溶液,故答案为:e;
②根据信息Ⅲ.在酸性条件下,Ca(NO2)2能将I-氧化为I2,S2O32-能将I2还原为I-。利用Ca(NO2)2的氧化性来测定其纯度,可以选择c1mol·L-1的KI溶液、淀粉溶液和稀硫酸以及c2mol·L-1的Na2S2O3溶液,步骤为准确称取mgCa(NO2)2样品放入锥形瓶中,加适量水溶解,加入过量c1mol·L-1的KI溶液、淀粉浓液,然后滴加稀硫酸,用c2mol·L-1的Na2S2O3溶液滴定至溶液由蓝色恰好变为无色,且半分钟内不变色,读取消耗Na2S2O3溶液的体积,重复以上操作23次,故答案为:加入过量c1mol·L-1的KI溶液、淀粉浓液,然后滴加稀硫酸,用c2mol·L-1的Na2S2O3溶液滴定至溶液由蓝色恰好变为无色,且半分钟内不变色,读取消耗Na2S2O3溶液的体积,重复以上操作23次。

 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案【题目】硼镁泥是硼镁矿生产硼砂晶体(Na2B4O7·10H2O)时的废渣,其主要成分是MgO,还含有Na2B4O7、CaO、Fe2O3、FeO、MnO、SiO2等杂质。以硼镁泥为原料制取七水硫酸镁的工艺流程如下:

回答下列问题:
(l)Na2B4O7·10H2O中B的化合价为__________。
(2)Na2B4O7易溶于水,也易发生水解:B4O72-+7H2O![]() 4H3BO3(硼酸)+2OH-(硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:______________。
4H3BO3(硼酸)+2OH-(硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:______________。
(3)滤渣B中含有不溶于稀盐酸但能溶于热浓盐酸的黑色固体,写出生成黑色固体的离子方程式____________。
(4)加入MgO的目的是___________________。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度(℃) 溶解度(g) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“操作A”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明“操作A”步骤为____________________。
(6)硼砂也能在工业上制取NaBH4,NaBH4被称为有机化学中的“万能还原剂”。
①写出NaBH4的电子式:___________。
②“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克H2的还原能力。NaBH4的有效氢含量为_________(保留两位小数)。
③在碱性条件下,在阴极上电解NaBO2也可制得硼氢化钠,写出阴极室的电极反应式:________。
【题目】草酸合铁酸钾晶体Kx[Fe(C2O4)y]·3H2O 是一种光敏材料,见光易分解,下面是一种制备草酸合铁酸钾晶体的实验流程。
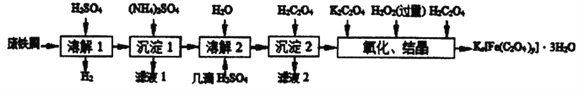
已知:(NH4)SO4、FeSO4·7H2O、莫尔盐[(NH4)2SO4·FeSO4·6H2O]的溶解度如表:
温度/℃ | 10 | 20 | 30 | 40 | 50 |
(NH4)SO4/g | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 |
FeSO4·7H2O/g | 40.0 | 48.0 | 60.0 | 73.3 | — |
(NH4)2SO4·FeSO4·6H2O/g | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 |
(1)废铁屑在进行“溶解1”前,得用在5%Na2CO3溶液中加热数分钟,并洗涤干净.Na2CO3溶液的作用是___________________。
(2)“复分解”制备莫尔盐晶体的基本实验步骤是: 蒸发浓缩、_________、过滤、用乙醇洗涤、干燥。用乙醇洗涤的目的是_________ 。
(3)“沉淀2"时得到的FeC2O4·2H2O 沉淀需用水洗涤干净.检验沉淀是否洗涤干净的方法是_____。
(4)“结晶”时应将溶液放在黑暗处等待晶体的析出,这样操作的原因是_________ 。
(5)为测定该晶体中铁的含量,某实验小组做了如下实验:
步骤1: 准确称量5.00g 草酸合铁酸钾晶体,配制成250mL 溶液
步骤2:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
步骤3:用0.010mol/L KMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液20.02mL,滴定中MnO4-被还原成Mn2+.重复步骤2、步骤3 操作,滴定消耗 0.010mol/LKMnO4溶液19.98mL,实验测得该晶体中铁的质量分数为_____ (写出计算过程)。