题目内容
12.CPAE是蜂胶的主要活性成分,也可由咖啡酸合成:下列说法不正确的是( )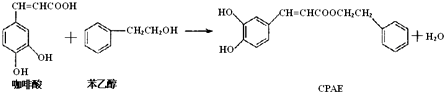
| A. | 咖啡酸分子中所有原子可能处在同一个平面上 | |
| B. | 1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH | |
| C. | 可用金属Na检测上述反应是否残留苯乙醇 | |
| D. | 1 mol 苯乙醇在O2中完全燃烧,需消耗10 mol O2 |
分析 A.苯环上所有碳原子处于同一平面上,乙烯中两个碳原子处于同一平面上;
B.酚-OH、-COOC-与NaOH溶液反应
C.Na与三种有机物均反应生成氢气;
D.苯乙醇的分子式为C8H10O,结合燃烧规律分析.
解答 解:苯环上所有碳原子处于同一平面上,乙烯中两个碳原子处于同一平面上,咖啡酸中含有苯环碳碳双键,所以所有碳原子可能处于同一平面上,故A正确;
B.酚-OH、-COOC-与NaOH溶液反应,则1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH,故B正确;
C.Na与三种有机物均反应生成氢气,则不能用金属Na检测上述反应是否残留苯乙醇,故C错误;
D.苯乙醇的分子式为C8H10O,1 mol 苯乙醇在O2中完全燃烧,需消耗1mol×(8+$\frac{10}{4}$-$\frac{1}{2}$)=10 mol O2,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高考常见题型,把握酚、醇、酯的性质为解答的关键,注意采用知识迁移的方法确定原子是否共面,题目难度中等.

练习册系列答案
相关题目
2.某强酸性溶液中可能存在Al3+、Fe2+、NH4+、Ba2+、Cl-、CO32-、SO42-、NO3-中的若干种,现取适量溶液进行如下实验

下列有关判断正确的是( )

下列有关判断正确的是( )
| A. | 原溶液中一定有Fe2+、SO42-、H+、NH4+、Al3+ | |
| B. | 原溶液中一定没有Ba2+、CO32-、NO3- | |
| C. | 步骤③中反应的离子方程式为2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- | |
| D. | 气体A、B之间肯定不能发生反应 |
20.下列叙述正确的是( )
①两种原子构成的共价化合物分子中的化学键都是极性键
②两种不同非金属元素原子间形成的化学键都是极性键
③含有非极性键的化合物一定是共价化合物,只要是离子化合物,其熔点就比共价化合物的熔点高
④难失去电子的原子,易形成阴离子
⑤单质分子中不存在化学键,化合物的分子中才存在化学键
⑥离子化合物中一定含有离子键.
①两种原子构成的共价化合物分子中的化学键都是极性键
②两种不同非金属元素原子间形成的化学键都是极性键
③含有非极性键的化合物一定是共价化合物,只要是离子化合物,其熔点就比共价化合物的熔点高
④难失去电子的原子,易形成阴离子
⑤单质分子中不存在化学键,化合物的分子中才存在化学键
⑥离子化合物中一定含有离子键.
| A. | 只有②⑥ | B. | 只有①⑥ | C. | 只有⑥ | D. | 只有①④⑥ |
7.有6种物质:①甲烷 ②甲苯 ③聚乙烯 ④丙烯⑤乙醇⑥乙醛,既能使酸性高锰酸钾溶液褪色又能与溴水起反应使之褪色的是( )
| A. | ②③④ | B. | ③④⑥ | C. | ②④⑤ | D. | ④⑥ |
4.下列排序不正确的是( )
| A. | 最高价氧化物对应水化物的酸性:H2SiO3>H3PO4>H2SO4 | |
| B. | 与冷水的反应速率:K>Na>Mg | |
| C. | 热稳定性:HF>HCl>H2S | |
| D. | 离子半径:Cl->F->Na+ |
1.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 1mol苯中碳碳双键的个数为3 NA | |
| B. | 含0.2molH2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA | |
| C. | 0.1mol/L的FeCl3溶液中含有0.1NA个Fe3+ | |
| D. | 在标准状况下,2.24 L NO和1.12 L O2混合后的原子总数为0.3 NA |
2.4p能级只填充一半电子的原子,其原子序数是( )
| A. | 15 | B. | 33 | C. | 35 | D. | 51 |
 .
. .
.