题目内容
【题目】原子序数依次增加的X、Y、Z、W四种元素原子序数均小于36,Y基态原子最外层电子数是其内层电子总数的3倍,X、W基态原子是同周期元素中未成对电子数最多的原子,X与Z的原子核内质子数之和等于W原子核内质子数,Z基态原子只有1个未成对的电子。回答下列问题:
(1)已知化合物XZ3与H2Y(Y的氢化物)发生反应的化学方程式为XZ3+H2Y→XH3+HZY,则元素的电负性:Y______Z(填“大于”或“小于”),化合物HZY分子的空间构型为______。
(2)X的一种氢化物的相对分子质量为32,1mol该氢化物中的σ键数是______。

(3)①元素Y的一种单质分子与元素X、Y形成的一种离子互为等电子体,这两种微粒的化学式是_______、________。
②基态W原子的电子排布式是_______________。
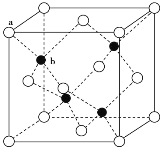
(4)元素Y和W的一种化合物的晶体结构如图所示,该晶体的化学式为______;金属原子______(选填“钾”、“镁”、“铜”)形成的晶体的堆积方式,与上述晶胞中Y离子的堆积方式相同。
【答案】大于 V形 5NA O3 NO2- 1s22s22p63s23p63d54s1或[Ar]3d54s1 Cr2O3 镁
【解析】
原子序数依次增加的X、Y、Z、W四种元素原子序数均小于36,Y基态原子最外层电子数是其内层电子总数的3倍,则Y为O元素;X、W基态原子是同周期元素中未成对电子数最多的原子,X原子序数比氧小,则X在第二周期为N元素;则W为第三周期的P或第四周期的Cr;已知X与Z的原子核内质子数之和等于W原子核内质子数,若W为P,则Z为O,与Y相同,所以不符合题意,若W为Cr,则Z为Cl,而且Cl的基态原子只有1个未成对的电子,符合题意,据此分析解答。
根据上述分析可知,X为N元素,Y为O元素,Z为Cl元素,W为Cr元素。
(1)化合物NCl 3与H2O发生反应的化学方程式为NCl 3+H2O→NH3+HClO,反应产物HClO中O元素为-2价,Cl元素为+1价,即O的得电子能力更强,所以电负性O大于Cl,HClO的结构为H-O-Cl,与H2O的H-O-H相似,是V形,故答案为:大于; V形;
(2)N的一种氢化物常见的有NH3和N2H4,相对分子质量为32的是N2H4,其结构式为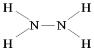 ,分子中含有5个σ键,所以1mol该氢化物中的σ键数是5NA,故答案为:5NA;
,分子中含有5个σ键,所以1mol该氢化物中的σ键数是5NA,故答案为:5NA;
(3)①元素O的一种单质分子与元素N、O形成的一种离子互为等电子体,O3 和NO2-的原子数和价电子数相同,互为等电子体,故答案为:O3 和NO2-;
②W为Cr元素,原子核外有24个电子,所以基态原子的电子排布式为1s22s22p63s23p63d54s1,故答案为:1s22s22p63s23p63d54s1或[Ar]3d54s1;
(4)由图可知,Cr离子位于晶胞内部,有4个,O2-位于上下面的面心和顶点,以及晶胞内部,所以O2-共有![]() ×2+
×2+![]() ×12+3=6个,则Cr与O的离子数之比为2∶3,所以该晶体的化学式为Cr2O3;由图可知,该晶胞为六方最密堆积,与Mg晶体的堆积方式相同,故答案为:Cr2O3;镁。
×12+3=6个,则Cr与O的离子数之比为2∶3,所以该晶体的化学式为Cr2O3;由图可知,该晶胞为六方最密堆积,与Mg晶体的堆积方式相同,故答案为:Cr2O3;镁。

【题目】下面是元素周期表的一部分,参照①~⑧元素在表中的位置,请用化学用语回答下列问题:
周期/主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)④、⑤、⑧三种元素中,离子半径大小的顺序为__________(填离子符号)。
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_________(填化学式)。
(3)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为:_____________。
(4)能说明⑧的非金属性比⑨的非金属性_________(填“强”或“弱”)的事实是____________________________(用离子方程式说明)。
(5)①和③形成的18电子的化合物甲是一种应用广泛的化工原料,写出甲的电子式:_________,实验室中可用次氯酸钠溶液与氨反应制备甲,反应的化学方程式为:____________________________。
【题目】工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7% O2:11% N2:82%)。
| 0.1个大气压 | 0.5个大气压 | 1个大气压 | 10个大气压 |
400 | 99.2 | 99.6 | 99.7 | 99.9 |
500 | 93.5 | 96.9 | 97.8 | 99.3 |
600 | 73.7 | 85.8 | 89.5 | 96.4 |
(1)SO2的氧化反应是___反应(填“吸热”或“放热”)。
(2)根据图中所给信息,你认为工业上将SO2转化为SO3的适宜条件是___。
(3)选择适宜的催化剂,是否可以提高SO2的转化率?___(填“是”或“否”)。
(4)若保持温度和容积不变,平衡后通入氧气,再达平衡时则SO2浓度___。(填“增大”或“减小”)
(5)若保持温度和压强不变,平衡后通入He气,SO3的含量___。(填“增大”或“减小”)
【题目】下表是不同温度下水的离子积数据:
温度/℃ | 25 | t1 | t2 |
水的离子积Kw | 1×10-14 | a | 1×10-12 |
试回答以下问题:
(1)若25<t1<t2,则a__1×10-14(填“>”“<”或“=”)。
(2)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4mol·L-1,取该溶液1 mL加水稀释至10mL,则稀释后溶液中c(Na+)∶c(OH-)=__。
(3)在t2℃下pH=10的NaOH溶液中,水电离产生的OH-浓度c(OH-)水=__。
(4)t2℃下,将pH=11的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=__。