题目内容
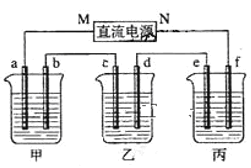
【题目】图所示装置中,甲、乙、丙三个烧杯依次分别盛放NaOH溶液、足量的CuSO4溶液和足量的 K2SO4溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加6.4g。以下说法不正确的是:
A.电源的N端为正极
B.电极b上发生的电极反应为4OH--4e-=2H2O+O2↑
C.b电极上生成气体1.12L,e电极上生成气体0.2 g
D.如果电解过程中铜全部析出,此时电解继续进行
【答案】C
【解析】
A、乙中c电极质量增加,则c处发生的反应为Cu2++2e-=Cu,即c处为阴极,由此可推出b为阳极,a为阴极,M为负极,N为正极,选项A正确;
B、甲中为NaOH溶液,相当于电解水,阳极b处为阴离子OH-放电,即4OH--4e-=2H2O+O2↑,选项B正确;
C、当乙中c电极质量增加6.4g时,根据Cu2++2e-=Cu可知转移0.2mol电子,电极b上发生的电极反应为4OH--4e-=2H2O+O2↑,则生成氧气0.05mol,标况下的体积为0.05mol×22.4L·mol-1=1.12L,但题中没说明标准状况,e电极上电极反应为2H++2e-=H2↑,生成气体0.1mol ![]() 2g/mol=0.2 g,选项C不正确;
2g/mol=0.2 g,选项C不正确;
D、如果电解过程中铜全部析出,则电解质溶液变为硫酸溶液,此时相当于电解水,电解继续进行,选项D正确。
答案选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目