题目内容
20.经测定某溶液中离子只有Na+、CH3COO-、H+、OH-四种,且离子浓度大小的排列顺序为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),则不可能的情形是( )| A. | 由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成 | |
| B. | 由0.2 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合而成 | |
| C. | 由0.1 mol/LCH3COOH溶液与等物质的量浓度等体积的NaOH溶液混合而成 | |
| D. | 向上述溶液中加入适量NaOH,可能使溶液中离子浓度大小改变为:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
分析 根据某溶液中离子只有Na+、CH3COO-、H+、OH-四种,离子浓度大小的排列顺序为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),则溶液显酸性,溶质不可能只有醋酸钠,则溶质可能为醋酸钠与醋酸,然后利用酸碱混合来分析溶液中的溶质即可解答.对于该溶液中加入碱,离子的浓度关系仍然遵循电荷守恒关系,则不会阴离子浓度都比阳离子浓度大.
解答 解:A、因pH=3的CH3COOH与pH=11的NaOH溶液等体积混合后溶液中的溶质为CH3COOH和CH3COONa,符合只有四种离子,且离子浓度c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故A正确;
B、因0.2mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合后溶液中的溶质为CH3COONa和CH3COOH,则c(OH-)<c(H+),c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故B正确;
C、因0.1mol/L的CH3COOH溶液与等物质的量浓度等体积的NaOH溶液混合后溶液的溶质为CH3COONa,则c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故C错误;
D、若加入NaOH后溶液中离子浓度大小为c(CH3COO-)>c(Na+)>c(OH-)>c(H+),则与电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(OH-)相矛盾,故D错误;
故选CD.
点评 本题考查酸碱混合后溶液中离子浓度的关系,明确酸碱混合后溶液中的溶质是解答的关键,并学会利用电荷守恒及盐类水解规律来分析溶液中的离子浓度的关系.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
10.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1molNa2O2与水完全反应时转移电子数为NA | |
| B. | 18g重水(D2O)所含的电子数为10NA | |
| C. | 0.5molNH4HSO4晶体中,含有H+数目约为0.5NA | |
| D. | 标准状况时,1LpH=13的NaOH溶液中含有的OH-离子数为0.1NA |
8.电视剧《活色生香》向我们充分展示了“香”的魅力.低级酯类化合物是具有芳香气味的液体,下列说法中,利用了酯的某种化学性质的是( )
| A. | 用酒精可以提取某些花香中的酯类香精,制成香水 | |
| B. | 炒菜时加一些料酒和食醋,使菜更香 | |
| C. | 用热水洗涤碗筷去油腻比冷水效果好 | |
| D. | 各种水果有不同的香味,是因为含有不同的酯 |
15.下列说法正确的是( )
| A. | 乳酸薄荷醇酯(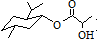 )只能发生水解、氧化、消去反应 )只能发生水解、氧化、消去反应 | |
| B. | 乙醛和丙烯醛不是同系物,它们的氢化产物也一定不是同系物 | |
| C. | 分子式为C7H14O2的有机物中,含3个甲基且能发生银镜反应还能发生水解反应的同分异构体数目是8个 | |
| D. | 硝化甘油、硝化纤维、硬脂酸甘油酯两两互不为同分异构体,其水解产物也完全不相同 |
5.铋酸钠(NaBiO3)溶液呈无色.向硫酸锰溶液中依次滴加下列溶液,对应的现象如表所示:
请比较实验中所有的氧化剂和氧化产物的氧化性强弱关系(反应过程中的涉及的气体均不参与比较):NaBiO3>NaMnO4>H2O2>I2.
| 加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水 | ③适量KI淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
12.为了探索外界条件对反应aX(g)+bY(g)?cZ(g)+Q的影响,以X和Y物质的量比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如下图所示.以下判断正确的是( )


| A. | Q<0,a+b>c | B. | Q<0,a+b<c | C. | Q>0,a+b>c | D. | Q>0,a+b<c |
9.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 11.2L氮气所含的分子数为0.5NA | |
| B. | 16g CH4含有的电子数为8NA | |
| C. | 7.8gNa2O2与足量CO2反应,转移的电子数为0.1NA | |
| D. | 1L0.1mol•L-1的Na2S溶液中含有的S2-为0.1 NA |
10.下列应用涉及氧化还原反应的是( )
| A. | 用食醋清洗烧水壶的水垢 | |
| B. | 用铝盐、铁盐作净水剂 | |
| C. | 用硫磺粉处理散落在地上的汞 | |
| D. | 用丁达尔现象区分食盐水和淀粉溶液 |