题目内容
18.在0.1mol/L(NH4)2SO4溶液中,离子浓度最大的是( )| A. | SO42- | B. | NH4+ | C. | H+ | D. | OH- |
分析 硫酸铵是强酸弱碱盐,硫酸铵在水溶液中电离出铵根离子和硫酸根离子,但铵根离子水解导致c(NH4+):c(SO42-)<2:1,但水解程度较小,据此分析解答.
解答 解:硫酸铵是强酸弱碱盐,硫酸铵在水溶液中电离出铵根离子和硫酸根离子,但铵根离子水解导致c(NH4+):c(SO42-)<2:1,溶液呈酸性,所以c(H+)>c(OH-),但水解程度较小,所以离子浓度大小顺序是c(NH4+)>c(SO42-)>c(H+)>c(OH-),则离子浓度最大的是铵根离子,故选B.
点评 本题以盐类水解为载体考查离子浓度大小比较,明确盐的类型及水解特点是解本题关键,注意铵根离子虽然水解但程度较小,题目难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
8.某小组利用如图装置,用苯与溴在FeBr3催化作用下制备溴苯:
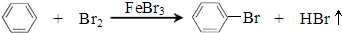
反应剧烈进行,烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现,蒸馏水逐渐变成黄色.反应停止后按 如下流程分离产品:
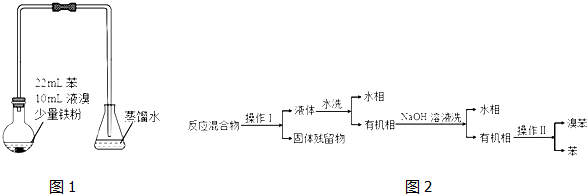
已知:
(1)操作Ⅰ为过滤,操作Ⅱ为蒸馏.
(2)“水洗”、“NaOH溶液洗”需要用到的玻璃仪器是分液漏斗、烧杯.
(3)“水洗”主要目的是除去FeBr3,“NaOH溶液洗”主要目的是除去Br2.
(4)锥形瓶中蒸馏水变黄的原因是溶解了从烧瓶中挥发出的溴.
(5)已知苯与溴发生的是取代反应,推测反应后锥形瓶中液体含有的两种大量离子是Br-、H+,请设计实验方案验证你的推测.(限选试剂:镁条、四氯化碳、氯水、溴水、蒸馏水)
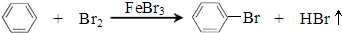
反应剧烈进行,烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现,蒸馏水逐渐变成黄色.反应停止后按 如下流程分离产品:

已知:
| 沸点℃ | 密度g/cm3 | 溶解性 | |
| 溴 | 59 | 3.119 | 水中溶解度小,易溶于有机溶剂 |
| 苯 | 80 | 0.8765 | 难溶于水,与有机溶剂互溶 |
| 溴苯 | 156 | 1.50 | 难溶于水,与有机溶剂互溶 |
(2)“水洗”、“NaOH溶液洗”需要用到的玻璃仪器是分液漏斗、烧杯.
(3)“水洗”主要目的是除去FeBr3,“NaOH溶液洗”主要目的是除去Br2.
(4)锥形瓶中蒸馏水变黄的原因是溶解了从烧瓶中挥发出的溴.
(5)已知苯与溴发生的是取代反应,推测反应后锥形瓶中液体含有的两种大量离子是Br-、H+,请设计实验方案验证你的推测.(限选试剂:镁条、四氯化碳、氯水、溴水、蒸馏水)
| 序号 | 实验步骤 | 预期现象 | 结论 |
| 1 | 将锥形瓶中液体转入分液漏斗,加入适量四氯化碳,振荡后分液.分别取少量上层无色溶液于试管A、B中 | ||
| 2 | 锥形瓶中液体含大量 Br- | ||
| 3 | 锥形瓶中液体含大量 H+ |
6.青石棉(cricidolite)是一种致癌物质,是《鹿特丹公约》中受限制的46种化学品之一,其化学式为:Na2Fe5Si8O22(OH)2.青石棉用稀硝酸溶液处理时,还原产物只有NO,下列说法不正确的是( )
| A. | 青石棉可能是一种硅酸盐 | |
| B. | 青石棉中含有一定量的石英晶体 | |
| C. | 青石棉能和18molHNO3反应 | |
| D. | 青石棉的化学组成可表示为:Na2O•3FeO•Fe2O3•8SiO2•H2O |
13.下列有机物名称中,符合系统命名法的是( )
| A. | 1,2,3-丙三醇 | B. | 1-甲基-5-乙基苯 | ||
| C. | 3-甲基-2-乙基戊烷 | D. | 2-甲基-1,3-丁二烯 |
3.X、Y、P、Q四种短周期元素,元素X在地壳中含量最高,充有元素Y单质蒸气的灯透雾能力强,常用于道路和广场的照明,Q的最外层电子数与其电子总数比为3:8,P的单质常用作电脑的芯片材料.下列说法正确的是( )
| A. | 元素Y、P的简单氢化物中化学键类型相同 | |
| B. | 原子半径:X>Y | |
| C. | 最高价氧化物的水化物酸性:P<Q | |
| D. | X、Q两元素的最高正化合价相同 |
10.下列各组数据中,其比值为2:1的是( )
| A. | 常温下,氨水与(NH4)2SO4溶液混合后pH=7的溶液中,c(NH4+):c(S042-) | |
| B. | 相同温度下,0.2 mo I•L-1乙酸溶液与0.1 mo I•L-1乙酸溶液中,c(H+)之比 | |
| C. | Na2C03溶液中,c(Na+):c(C032-) | |
| D. | 常温下,pH=12的Ba(OH)2溶液与pH=12的KOH溶液中,c[Ba(OH)2]:c(KOH) |
7.下列各组物质中,所含分子数相同的是( )
| A. | 10g O2和10gH2 | B. | 5.6LN2(标准状况)和11gCO2 | ||
| C. | 9gH2O和0.5molBr2 | D. | 224mL H2(标准状况)和0.1molN2 |