题目内容
在氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质.下列实验现象和结论一致且正确的是( )
| A、加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在 |
| B、滴入石蕊,先变红,后褪色,说明溶液中有H+和HClO分子存在 |
| C、先用盐酸酸化,再加入AgNO3溶液产生白色沉淀,说明有Cl-存在 |
| D、加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在 |
考点:氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:新制氯水中存在Cl2+H2O?H++Cl-+HClO,所含分子只有Cl2和H2O、HClO分子,所含的离子只有H+、Cl-、ClO-和OH-,结合对应离子的性质解答该题.
解答:
解:A.氯水中含有次氯酸,可使有色布条褪色,故A错误;
B.氯气和水反应生成盐酸和次氯酸,其中H+可使石蕊变红,HClO可使石蕊褪色,故B正确;
C.加入盐酸,引入氯离子,不能确定氯水中含有Cl-,故C错误;
D.加入NaOH溶液,氯水浅黄绿色消失,是由于氯气和氢氧化钠溶液反应,与次氯酸无关,故D错误.
故选B.
B.氯气和水反应生成盐酸和次氯酸,其中H+可使石蕊变红,HClO可使石蕊褪色,故B正确;
C.加入盐酸,引入氯离子,不能确定氯水中含有Cl-,故C错误;
D.加入NaOH溶液,氯水浅黄绿色消失,是由于氯气和氢氧化钠溶液反应,与次氯酸无关,故D错误.
故选B.
点评:本题考查氯水的成分及氯水中各微粒的性质,为高频考点,侧重于学生的分析能力的考查,明确离子、分子的性质是解答本题的关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在一定温度下,向容积固定不变的密闭容器中充入a mol A,发生反应:2A(g)?B(g);△H<0.达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
| A、相对平均分子质量增大 |
| B、A的转化率提高 |
| C、A的质量分数增大 |
| D、反应放出的总热量大于原来的2倍 |
将1mol冰醋酸加入到一定量的蒸馏水中最终得到1L溶液.下列各项中表征醋酸已达到电离平衡状态的是( )
| A、醋酸的浓度达到1mol?L-1 |
| B、H+的浓度达到0.5mol?L-1 |
| C、醋酸的浓度、醋酸根离子的浓度、H+的浓度均为0.5mol?L-1 |
| D、醋酸分子电离成离子的速率和离子重新结合成分子的速率相等 |
一定条件下某容器中各微粒在反应前后的变化如图所示,其中●和○代表不同元素的原子.关于此反应说法错误的是( )


| A、一定属于可逆反应 |
| B、一定属于化合反应 |
| C、一定属于氧化还原反应 |
| D、一定属于放热反应 |
下列各组离子,在指定环境中能大量共存的是( )
| A、常温下,在PH>7的溶液中,Na+、S2-、K+、AlO2- |
| B、常温下,在PH>1的溶液中,SO32-、S2-、K+、NH4+ |
| C、常温下,在PH=1的溶液中,Fe2+、HCO3-、Na+、SO42- |
| D、常温下,在PH<7的溶液中,Fe3+、Cu2+、Cl-、NO3- |
电化学在日常生活中用途广泛,下图①是镁、次氯酸钠燃料电池的示意图,电池总反应式为:Mg+ClO-+H2O═Cl-+Mg(OH)2↓,图②是含Cr2O72-工业废水的电化学处理示意图.下列说法正确的是( )
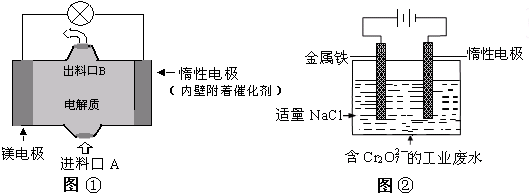

| A、图②中Cr2O72-离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 |
| B、图②中阳极上的电极反应式为:Fe-3e-═Fe3+ |
| C、图①中发生的还原反应是:Mg2++ClO-+H2O+2e-═Cl-+Mg (OH)2↓ |
| D、若图①中3.6g镁溶解产生的电量用以图②废水处理,理论可产生10.7g氢氧化铁沉淀 |
设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A、标准状况下,22.4L氦气中含有的电子数为2NA |
| B、11g的2H218O分子中含NA个中子 |
| C、1mol NH4+离子所含的质子总数为10NA |
| D、电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g |
离子方程式H++OH-=H2O可表示的化学方程式是( )
| A、盐酸与氢氧化铜的反应 |
| B、硫酸与氢氧化钠的反应 |
| C、硫酸与氢氧化镁的反应 |
| D、盐酸与氨水的反应 |
下列溶液中的Cl-浓度与50mL 1mol/L MgCl2溶液中的Cl-浓度相等的是( )
| A、150mL 2mol/L KCl溶液 |
| B、75mL 1mol/L CaCl2溶液 |
| C、150mL 1mol/L NaCl溶液 |
| D、75mL 1mol/L AlCl3溶液 |