题目内容
下列各组离子,在指定环境中能大量共存的是( )
| A、常温下,在PH>7的溶液中,Na+、S2-、K+、AlO2- |
| B、常温下,在PH>1的溶液中,SO32-、S2-、K+、NH4+ |
| C、常温下,在PH=1的溶液中,Fe2+、HCO3-、Na+、SO42- |
| D、常温下,在PH<7的溶液中,Fe3+、Cu2+、Cl-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.常温下,在PH>7的溶液中存在大量的氢氧根离子,Na+、S2-、K+、AlO2-离子之间不发生反应,也不与氢氧根离子反应,在溶液中能够大量共存;
B.常温下,在PH>1的溶液中存在大量的氢离子或氢氧根离子,SO32-、S2-能够与氢离子反应,铵根离子能够与氢氧根离子反应;
C.常温下,在PH=1的溶液中存在大量的氢离子,碳酸氢根离子能够与氢离子反应,亚铁离子能够与碳酸氢根离子发生双水解反应;
D.常温下,在PH<7的溶液中存在大量氢离子,Fe3+、Cu2+、Cl-、NO3-离子之间不发生反应,也不与氢离子反应.
B.常温下,在PH>1的溶液中存在大量的氢离子或氢氧根离子,SO32-、S2-能够与氢离子反应,铵根离子能够与氢氧根离子反应;
C.常温下,在PH=1的溶液中存在大量的氢离子,碳酸氢根离子能够与氢离子反应,亚铁离子能够与碳酸氢根离子发生双水解反应;
D.常温下,在PH<7的溶液中存在大量氢离子,Fe3+、Cu2+、Cl-、NO3-离子之间不发生反应,也不与氢离子反应.
解答:
解:A.常温下,在PH>7的溶液为碱性溶液,Na+、S2-、K+、AlO2-之间不反应,也不与OH-离子反应,在溶液中能够大量共存,故A正确;
B.常温下,在PH>1的溶液可能为酸性或者碱性溶液,SO32-、S2-能够与H+反应,NH4+离子能够与OH-反应,在溶液中不能大量共存,故B错误;
C.常温下,在PH=1的溶液为酸性溶液,Fe2+、H+与HCO3-离子发生反应,在溶液中不能大量共存,故C错误;
D.常温下,在PH<7的溶液为酸性溶液,Fe3+、Cu2+、Cl-、NO3-离子之间不反应,也不与H+发生反应,在溶液中能够大量共存,故D正确;
故选AD.
B.常温下,在PH>1的溶液可能为酸性或者碱性溶液,SO32-、S2-能够与H+反应,NH4+离子能够与OH-反应,在溶液中不能大量共存,故B错误;
C.常温下,在PH=1的溶液为酸性溶液,Fe2+、H+与HCO3-离子发生反应,在溶液中不能大量共存,故C错误;
D.常温下,在PH<7的溶液为酸性溶液,Fe3+、Cu2+、Cl-、NO3-离子之间不反应,也不与H+发生反应,在溶液中能够大量共存,故D正确;
故选AD.
点评:本题考查离子共存的正误判断,题目难度中等,注意明确离子不能大量共存的一般情况,如:能生成难溶物的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图所示实验合理的是( )
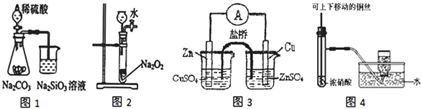

| A、图1证明非金属性强弱:S>C>Si |
| B、图2可制备少量氧气 |
| C、图3构成铜锌原电池,产生持续稳定的电流 |
| D、图4可制备并收集NO2气体 |
正确掌握好化学用语是学好化学的基础,下列有关表述正确的是( )
A、次氯酸的电子式: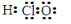 |
| B、碳酸氢根离子的电离方程式:HCO3-+H2O?H3O++CO32- |
C、乙烯的结构简式: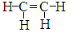 |
| D、质量数为16的氧原子:168O |
下列反应属于取代反应的是( )
A、2CH3CHO+O2
| ||||
B、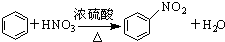 | ||||
C、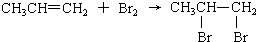 | ||||
D、nCH2=CH2
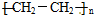 |
在氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质.下列实验现象和结论一致且正确的是( )
| A、加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在 |
| B、滴入石蕊,先变红,后褪色,说明溶液中有H+和HClO分子存在 |
| C、先用盐酸酸化,再加入AgNO3溶液产生白色沉淀,说明有Cl-存在 |
| D、加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在 |
下列化学用语表示正确的是( )
A、CO(NH2)2的电子式: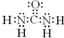 |
| B、NaHCO3的电离方程式:NaHCO3═Na++H++CO32- |
| C、1-丙醇的结构简式:C3H7OH |
| D、含18个中子的氯原子的核素符号:3517Cl |
下列各组物质充分反应后,滴入KSCN溶液一定显红色的是( )
| A、FeO放入稀HCl中 |
| B、FeCl3、CuCl2的混合溶液中加入过量的铁粉 |
| C、Fe(NO3)2固体溶于稀H2SO4中 |
| D、Fe放入HNO3溶液中 |
对体积不变的气体反应,升高温度时,化学反应速率加快,主要原因是( )
| A、分子运动速率加快,使反应物分子间的碰撞机会增多 |
| B、反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
| C、该反应的过程是吸热的 |
| D、该反应的过程是放热的 |