题目内容
设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A、标准状况下,22.4L氦气中含有的电子数为2NA |
| B、11g的2H218O分子中含NA个中子 |
| C、1mol NH4+离子所含的质子总数为10NA |
| D、电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.稀有气体为单原子,1mol氦气分子中含有1mol氦原子,含有2mol电子;
B.2H218O分子的摩尔质量为22g/mol,该水分子中含有12个中子;
C.铵根离子中含有11个质子,1mol铵根离子中含有11mol质子;
D.粗铜中含有杂质铁、锌,电解过程中铁、锌等 杂质优先放电,阳极减少的铜减少.
B.2H218O分子的摩尔质量为22g/mol,该水分子中含有12个中子;
C.铵根离子中含有11个质子,1mol铵根离子中含有11mol质子;
D.粗铜中含有杂质铁、锌,电解过程中铁、锌等 杂质优先放电,阳极减少的铜减少.
解答:
解:A.标况下22.4L氦气的物质的量为1mol,1mol氦气中含有1mol氦原子,1mol氦原子含有2mol电子,含有的电子数为2NA,故A正确;
B.11g2H218O分子的物质的量为0.5mol,0.5mol该重水中含有6mol中子,含6NA个中子,故B错误;
C.1mol铵根离子中含有11mol质子,所含的质子总数为11NA,故C错误;
D.电解精炼铜时,若阴极得到电子数为2NA个,转移的电子为2mol,由于阳极放电的不只有铜,还有杂质铁、锌等杂质,所以阳极减少的铜小于1mol,质量小于64g,故D错误;
故选A.
B.11g2H218O分子的物质的量为0.5mol,0.5mol该重水中含有6mol中子,含6NA个中子,故B错误;
C.1mol铵根离子中含有11mol质子,所含的质子总数为11NA,故C错误;
D.电解精炼铜时,若阴极得到电子数为2NA个,转移的电子为2mol,由于阳极放电的不只有铜,还有杂质铁、锌等杂质,所以阳极减少的铜小于1mol,质量小于64g,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确需要气态为单原子分子,选项D为易错点,注意粗铜中含有活泼性较强铁、锌等杂质.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
如果我们规定12C的相对原子质量为24,且0.024kg 12C中所含的原子个数为阿伏加德罗常数(NA),那么下列几种物理量(1)一个12C原子的质量;(2)阿伏加德罗常数(NA);(3)摩尔质量;(4)O2的相对分子质量;(5)气体摩尔体积;(6)agC2H5OH的物质的量;(7)98%浓硫酸的物质的量浓度;(8)44g CO2所含的分子个数.没有变化的是( )
| A、(1) |
| B、(1)(6)(7)(8) |
| C、(2)(3)(4)(5) |
| D、(1)(8) |
正确掌握好化学用语是学好化学的基础,下列有关表述正确的是( )
A、次氯酸的电子式: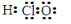 |
| B、碳酸氢根离子的电离方程式:HCO3-+H2O?H3O++CO32- |
C、乙烯的结构简式: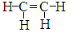 |
| D、质量数为16的氧原子:168O |
在氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质.下列实验现象和结论一致且正确的是( )
| A、加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在 |
| B、滴入石蕊,先变红,后褪色,说明溶液中有H+和HClO分子存在 |
| C、先用盐酸酸化,再加入AgNO3溶液产生白色沉淀,说明有Cl-存在 |
| D、加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在 |
下列化学用语表示正确的是( )
A、CO(NH2)2的电子式: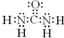 |
| B、NaHCO3的电离方程式:NaHCO3═Na++H++CO32- |
| C、1-丙醇的结构简式:C3H7OH |
| D、含18个中子的氯原子的核素符号:3517Cl |
下列叙述中,错误的是( )
| A、苯与浓硝酸、浓硫酸共热并保持55-60℃反应生成硝基苯 |
| B、苯乙烯在合适条件下催化加氢可生成乙基环己烷 |
| C、甲苯与氯气在光照下反应主要生成2,4-二氯甲苯 |
| D、乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 |
下列各组物质充分反应后,滴入KSCN溶液一定显红色的是( )
| A、FeO放入稀HCl中 |
| B、FeCl3、CuCl2的混合溶液中加入过量的铁粉 |
| C、Fe(NO3)2固体溶于稀H2SO4中 |
| D、Fe放入HNO3溶液中 |
下列各组离子,在溶液中可以大量共存的是( )
| A、Na+ Ca2+ Cl- CO32- |
| B、K+ NH4+ SO42- NO3- |
| C、Na+ H+ Cl- OH- |
| D、Ba2+ Ca2+ Cl- SO42- |
铅蓄电池用途极广,可多次充放电.铅蓄电池中铅做负极,二氧化铅做正极,电解液为30%的H2SO4溶液.电池充、放电时的总反应可表示为:Pb+PbO2+2H2SO4
2PbSO4+2H2O,下列关于此电池的说法中,不正确的是( )
| 放电 |
| 充电 |
| A、放电一段时间后,电解液的pH将增大 |
| B、放电时,铅电极上发生的电极反应式为:Pb+SO42--2e-═PbSO4 |
| C、充电时,原来材料为二氧化铅的电极上发生氧化反应 |
| D、充电时,电解液中的阳离子向原来材料为二氧化铅的电极移动 |