题目内容
17.下列有关物质的性质与应用相对应的是( )| A. | 浓硫酸具有吸水性,可用于干燥二氧化碳、硫化氢等气体 | |
| B. | 氨气极易溶于水,可用作制冷剂 | |
| C. | 浓硝酸在常温下能使铝钝化,可用铝槽车运输浓硝酸 | |
| D. | SO2具有强还原性,在空气中极易被氧化为SO3 |
分析 A、硫化氢气体具有还原性,而浓硫酸具有氧化性;
B、氨气极易液化,可作制冷剂;
C、浓硝酸具有强氧化性,能使铝钝化;
D、二氧化硫要在催化剂条件下才能氧化成三氧化硫.
解答 解:A、硫化氢气体具有还原性,而浓硫酸具有氧化性,所以不能用浓硫酸干燥,故A错误;
B、氨气极易液化,可作制冷剂,而不极易溶于水,故B错误;
C、浓硝酸具有强氧化性,能使铝钝化,则可用铝槽车运输浓硝酸,故C正确;
D、二氧化硫要在催化剂条件下才能氧化成三氧化硫,所以SO2在空气中不易被氧化成三氧化硫,故D错误;
故选C.
点评 本题考查了硫酸和二氧化硫的性质,注意浓硫酸的强氧化性酸,与活泼金属反应不生成氢气,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列分子中,所有原子都处在同一平面的是( )
| A. | 丙炔 | B. | 乙烯 | C. | 乙烷 | D. | 苯 |
5.化合物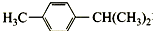 在核磁共振氢谱图中各信号的面积比为( )
在核磁共振氢谱图中各信号的面积比为( )
 在核磁共振氢谱图中各信号的面积比为( )
在核磁共振氢谱图中各信号的面积比为( )| A. | 3:4:1:3:3 | B. | 3:2:2:1:6 | C. | 9:4:1 | D. | 3:4:7 |
12.下列对化合物M、N的叙述正确的是( )


| A. | M的分子式为C12H9O3 | |
| B. | 1mol M在最多能与6molH2发生加成反应 | |
| C. | M与N可用试剂组合:溴水、NaOH溶液鉴别 | |
| D. | M与N可用试剂组合:FeCl3溶液、稀H2SO4鉴别 |
2.将3.2g铜与过量浓硫酸共热反应,下列叙述中错误的是( )
| A. | 生成的气体体积为1.12 L | |
| B. | 铜片溶解,生成物冷却后倒入盛有水的烧杯中,溶液成蓝色 | |
| C. | 参加反应的硫酸与被还原的硫酸物质的量之比为2:1 | |
| D. | 该实验中可用Na2CO3溶液处理尾气 |
9.常温下pH最小的是下列各项中的( )
| A. | pH=0的溶液 | B. | 0.04 mol•L-1H2SO4 | ||
| C. | 0.5 mol•L-1HCl | D. | 0.05 mol•L-1CH3COOH |
7.化合物A、B、C、D各由两种元素组成,甲、乙、丙是短周期元素的三种单质.这些常见的化合物与单质之间存在如下关系(已知C是一种有机物),以下结论不正确的是( )


| A. | 常温下,甲、乙、丙三种单质均为气体 | |
| B. | 上述转化关系所涉及的化合物中有一种是电解质 | |
| C. | 上图所示的五个转化关系中,有三个是化合反应 | |
| D. | 上图所示的五个转化关系中,均为氧化还原反应 |
 I.
I.