题目内容
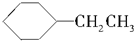
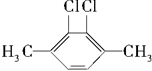
5.化合物 在核磁共振氢谱图中各信号的面积比为( )
在核磁共振氢谱图中各信号的面积比为( )| A. | 3:4:1:3:3 | B. | 3:2:2:1:6 | C. | 9:4:1 | D. | 3:4:7 |
分析 核磁共振氢谱中有几个不同的信号,分子中就有几种H原子,信号的面积之比等于氢原子数之比,利用等效氢原子判断:①分子中同一甲基上连接的氢原子等效;②同一碳原子所连甲基上的氢原子等效,同一同一碳原子所连氢原子等效;③处于镜面对称位置上的氢原子等效.
解答 解:化合物中含有5种氢原子: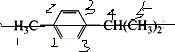 ,氢原子的个数分别为:3、2、2、1、6,各信号的面积比为3:2:2:1:6,故选B.
,氢原子的个数分别为:3、2、2、1、6,各信号的面积比为3:2:2:1:6,故选B.
点评 本题以核磁共振氢谱为载体考查等效氢原子,难度较小,清楚核磁共振氢谱中有几个不同的信号,分子中就有几种H原子.

练习册系列答案
相关题目
16.高锰酸钾[KMnO4]是常用的氧化剂.工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体.中间产物为锰酸钾[K2MnO4].如图1是实验室模拟制备的操作流程:
相关资料:
①物质溶解度
②锰酸钾[K2MnO4]外观性状:墨绿色结晶.其水溶液呈深绿色,这是锰酸根(MnO42-)的特征颜色.
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42-会发生歧化反应.
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是高温下强碱会和瓷坩埚中的二氧化硅反应腐蚀坩埚;实验中用铁坩埚煅烧暴露在空气中的固体混合物发生反应的化学方程式为2MnO2+4KOH+O2$\frac{\underline{\;高温\;}}{\;}$2K2MnO4+2H2O.
(2)实验时,若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低.请写出实验中通入适量CO2时体系中可能发生反应离子方程式:3MnO42-+2CO2═2MnO4-+MnO2↓+2CO32-,2OH-+CO2═CO32-+H2O;其中氧化还原反应中氧化剂和还原剂的质量比为1:2.
(3)由于CO2的通人量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸.从理论上分析,选用下列酸中A,得到的产品纯度更高.
A.醋酸 B.浓盐酸 C.稀硫酸
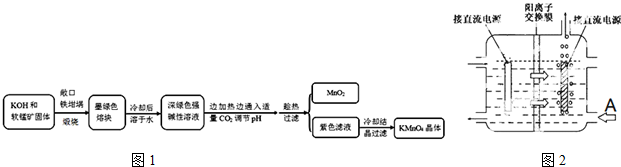
(4)工业上一般采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程式2K2MnO4+2H2O$\frac{\underline{\;高温\;}}{\;}$2KMnO4+H2↑+2KOH;
传统工艺采用无膜电解法由于副反应发生,Mn元素利用率和电流效率都会偏低.有同学联想到离子交换膜法电解饱和食盐水提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图2).图中A口加入的溶液最好为KOH溶液.使用阳离子交换膜可以提高Mn元素利用率的原因为阳离子交换膜防止锰酸根进入阴极区被还原.

相关资料:
①物质溶解度
| 物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
| 20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42-会发生歧化反应.
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是高温下强碱会和瓷坩埚中的二氧化硅反应腐蚀坩埚;实验中用铁坩埚煅烧暴露在空气中的固体混合物发生反应的化学方程式为2MnO2+4KOH+O2$\frac{\underline{\;高温\;}}{\;}$2K2MnO4+2H2O.
(2)实验时,若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低.请写出实验中通入适量CO2时体系中可能发生反应离子方程式:3MnO42-+2CO2═2MnO4-+MnO2↓+2CO32-,2OH-+CO2═CO32-+H2O;其中氧化还原反应中氧化剂和还原剂的质量比为1:2.
(3)由于CO2的通人量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸.从理论上分析,选用下列酸中A,得到的产品纯度更高.
A.醋酸 B.浓盐酸 C.稀硫酸
(4)工业上一般采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程式2K2MnO4+2H2O$\frac{\underline{\;高温\;}}{\;}$2KMnO4+H2↑+2KOH;
传统工艺采用无膜电解法由于副反应发生,Mn元素利用率和电流效率都会偏低.有同学联想到离子交换膜法电解饱和食盐水提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图2).图中A口加入的溶液最好为KOH溶液.使用阳离子交换膜可以提高Mn元素利用率的原因为阳离子交换膜防止锰酸根进入阴极区被还原.
13.下列做法与化学反应速率有关的是( )
| A. | 把块状固体反应物研成粉末 | B. | 使用合适的催化剂 | ||
| C. | 增加反应物的浓度 | D. | 改变反应的温度 |
10.下列对丙酸和甲酸乙酯的说法中,错误的是( )
| A. | 它们互为同分异构体 | B. | 沸点较高的是甲酸乙酯 | ||
| C. | 它们可用红外光谱法鉴别 | D. | 它们可用KMnO4(H+)溶液鉴别 |
17.下列有关物质的性质与应用相对应的是( )
| A. | 浓硫酸具有吸水性,可用于干燥二氧化碳、硫化氢等气体 | |
| B. | 氨气极易溶于水,可用作制冷剂 | |
| C. | 浓硝酸在常温下能使铝钝化,可用铝槽车运输浓硝酸 | |
| D. | SO2具有强还原性,在空气中极易被氧化为SO3 |
14.下列各组物质中属于同分异构体的是( )
| A. | H2O和D2O | B. | 甲醇和二甲醚CH3-O-CH3 | ||
| C. | 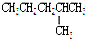 和 和 | D. | 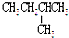 和 和 |
15.下列物质可以使蛋白质变性的是:( )
①福尔马林 ②酒精 ③紫外线照射 ④(NH4)22SO4 ⑤CuSO4 ⑥双氧水 ⑦硝酸.
①福尔马林 ②酒精 ③紫外线照射 ④(NH4)22SO4 ⑤CuSO4 ⑥双氧水 ⑦硝酸.
| A. | 除④外 | B. | 除③、⑥外 | C. | ①②⑤ | D. | 除④、⑦外 |