题目内容
9.常温下pH最小的是下列各项中的( )| A. | pH=0的溶液 | B. | 0.04 mol•L-1H2SO4 | ||
| C. | 0.5 mol•L-1HCl | D. | 0.05 mol•L-1CH3COOH |
分析 溶液的pH=-lgc(H+),则溶液中氢离子浓度越大,则溶液的pH越小,先判断溶液的酸碱性,酸溶液的pH一定<碱性溶液的pH;常温下pH最小,说明溶液中氢离子浓度最大、酸性最强,据此进行解答.
解答 解:A.常温下pH=0的溶液中氢离子浓度为1mol/L;
B.硫酸为强电解质,0.04 mol•L-1H2SO4溶液中氢离子浓度为:0.04mol/L×2=0.08mol/L;
C.氯化氢为强电解质,0.5mol/L的氯化氢溶液中,氢离子浓度为0.5mol/L;
D.醋酸为弱酸,0.05mol/L的醋酸溶液中,氢离子浓度一定小于0.05mol/L;
根据分析可知,溶液中氢离子浓度最大的为A,该溶液的pH最小,
故选A.
点评 本题考查了溶液酸碱性与溶液pH的关系及计算,题目难度不大,明确溶液pH的表达式及计算方法为解答关键,注意掌握溶液酸碱性与溶液pH的关系.

练习册系列答案
相关题目
19.下列说法正确的是( )
| A. | 分子式相同的不同物质一定是同分异构体 | |
| B. | 通式相同的不同物质一定属于同系物 | |
| C. | 相对分子质量相同的不同物质一定是同分异构体 | |
| D. | 分子式相同,元素的质量分数也相同的物质是同种物质 |
17.下列有关物质的性质与应用相对应的是( )
| A. | 浓硫酸具有吸水性,可用于干燥二氧化碳、硫化氢等气体 | |
| B. | 氨气极易溶于水,可用作制冷剂 | |
| C. | 浓硝酸在常温下能使铝钝化,可用铝槽车运输浓硝酸 | |
| D. | SO2具有强还原性,在空气中极易被氧化为SO3 |
4.已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系如图.甲和X不可能是( )
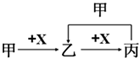
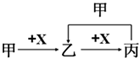
| A. | 甲为C,X为O2 | B. | 甲为Fe,X为Cl2 | ||
| C. | 甲为SO2,X为NaOH溶液 | D. | 甲为Fe,X为稀硝酸溶液 |
14.下列各组物质中属于同分异构体的是( )
| A. | H2O和D2O | B. | 甲醇和二甲醚CH3-O-CH3 | ||
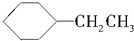
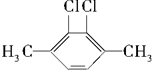
| C. | 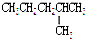 和 和 | D. |  和 和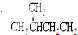 |
1.已知元素的原子序数,可以推知原子的①原子数②核电荷数③核外电子数④在周期表中的位置,其中正确的是( )
| A. | ①③ | B. | ②③ | C. | ①②③ | D. | ②③④ |
18.四位同学在一起讨论某种物质,请根据他们的讨论判断该物质是( )


| A. | Na2CO3 | B. | CaCO3 | C. | CaCl2 | D. | NaHCO3 |
19.下列物质不属于电解质的是( )
| A. | BaCl2 | B. | KOH | C. | HNO3 | D. | C2H5OH |