题目内容
18.已知CH3CH2Cl+NaOH$→_{△}^{醇}$CH═CH2+NaCl+H2O(消去反应).某烃A与Br2发生加成反应,产生二溴衍生物B;B用热的NaOH-乙醇溶液处理得到化合物C;经测试知C的化学式中含有两个双键,化学式是C5H6;将C催化加氢生成环戊烷.(1)写出A发生加聚反应的化学方程式n
 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$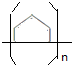 .
.(2)写出B→C反应的化学方程式
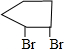 +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$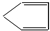 +2NaBr+2H2O.
+2NaBr+2H2O.(3)写C与等物质的量Br2发生加成反应的化学方程式
 +Br2→
+Br2→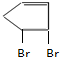 、
、 +Br2→
+Br2→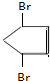 .
.
分析 烃A和溴发生加成反应生成二溴衍生物B,说明A是烯烃,B用热的NaOH乙醇溶液处理得到化合物C,经测试知C的化学式中含有两个双键,则B发生消去反应生成C,C的化学式为C5H6,将C催化加氢生成环戊烷,则C结构简式为 ,B为
,B为 、则A为
、则A为 ,结合题目分析解答.
,结合题目分析解答.
解答 解:烃A和溴发生加成反应生成二溴衍生物B,说明A是烯烃,B用热的NaOH乙醇溶液处理得到化合物C,经测试知C的化学式中含有两个双键,则B发生消去反应生成C,C的化学式为C5H6,将C催化加氢生成环戊烷,则C结构简式为 ,B为
,B为 、则A为
、则A为 ,
,
(1)A为 ,A发生加聚反应的化学方程式为n
,A发生加聚反应的化学方程式为n $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ ,
,
故答案为:n $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ ;
;
(2)C为 ,B为
,B为 ,B和氢氧化钠的醇溶液共热得到C,B→C反应的化学方程式为
,B和氢氧化钠的醇溶液共热得到C,B→C反应的化学方程式为 +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$ +2NaBr+2H2O,
+2NaBr+2H2O,
故答案为: +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$ +2NaBr+2H2O;
+2NaBr+2H2O;
(3)C与等物质的量Br2发生加成反应的化学方程式为 +Br2→
+Br2→ 、
、 +Br2→
+Br2→ ,
,
故答案为: +Br2→
+Br2→ ;
; +Br2→
+Br2→ .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,以环戊烷为突破口结合反应条件、某些物质结构进行推断,注意(3)中二烯烃发生加成反应特点,题目难度不大.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
8.X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族,其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.下列说法不正确的是( )
| A. | 原子半径:Y>Z>W | |
| B. | ZW2电子式为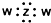 | |
| C. | 片状Y在空气中点燃时现象不剧烈 | |
| D. | 已知XW2熔点为-107℃、沸点为12.5℃,熔融时不导电,可说明固态XW2为共价化合物 |
9.下列说法正确的是( )
①Na2CO3-制玻璃; ②SiO2-太阳能电池;③AgI-人工降雨;④Fe2O3-红色油漆或涂料;
⑤Al2O3-焊接钢轨;⑥NaClO-消毒剂; ⑦NaCl-制纯碱;⑧明矾-用于水的消毒、杀菌.
①Na2CO3-制玻璃; ②SiO2-太阳能电池;③AgI-人工降雨;④Fe2O3-红色油漆或涂料;
⑤Al2O3-焊接钢轨;⑥NaClO-消毒剂; ⑦NaCl-制纯碱;⑧明矾-用于水的消毒、杀菌.
| A. | ①②③⑥⑧ | B. | ②③⑤⑥⑦ | C. | ②③④⑥⑧ | D. | ①③④⑥⑦ |
6.下列说法中,不正确的是( )
| A. | 若反应时形成新化学键释放的能量大于断裂旧化学键所吸收的能量,则该化学反应是释放能量的反应 | |
| B. | 若反应物的总能量大于生成物的总能量,则该化学反应为释放能量的反应 | |
| C. | 化学反应中能量变化的大小与反应物的质量多少无关 | |
| D. | 化学反应必然伴随着能量的变化 |
13.某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理.
(1)请写出SO2与过量NaOH溶液反应的离子方程式:SO2+2OH-=H2O+SO32-.
(2)吸收尾气(Cl2)一段时间后,吸收液(强碱性)中肯定存在的阴离子有OH-和Cl-、SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响)
①提出合理假设.
假设1:只存在SO32-
假设2:既不存在SO32-,也不存在ClO-;
假设3:两种离子都存在(或者 只存在ClO-);.
②要证明假设1是否成立,设计实验方案,进行实验.请写出实验以及预期现象和结论.限选实验试剂:3mol•L-1H2SO4、1mol•L-1NaOH、0.01mol•L-1KMnO4、淀粉-KI溶液.
(1)请写出SO2与过量NaOH溶液反应的离子方程式:SO2+2OH-=H2O+SO32-.
(2)吸收尾气(Cl2)一段时间后,吸收液(强碱性)中肯定存在的阴离子有OH-和Cl-、SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响)
①提出合理假设.
假设1:只存在SO32-
假设2:既不存在SO32-,也不存在ClO-;
假设3:两种离子都存在(或者 只存在ClO-);.
②要证明假设1是否成立,设计实验方案,进行实验.请写出实验以及预期现象和结论.限选实验试剂:3mol•L-1H2SO4、1mol•L-1NaOH、0.01mol•L-1KMnO4、淀粉-KI溶液.
| 实验 | 预期现象和结论 |
| 取少许吸收液于试管中滴加1~2滴0.01mol•L-1KMnO4溶液 | 若溶液褪色则假设1成立,否则假设1不成立 |
3.某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验目的:探究同一周期主族元素性质的递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液等.仪器:①烧杯,②试管,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
(4)若用最高价氧化物的水化物的碱性相对强弱来验证Mg、Al失电子能力的相对强弱,请你设计实验(实验用品自选,不要求写化学方程式):向溶液中滴加NaOH溶液至过量,得白色沉淀,不溶解;向溶液中滴加NaOH溶液至过量,产生白色胶状沉淀,继而沉淀消失;.
(5)实验结论:同周期元素随原子序数增大,元素金属性逐渐减弱,非金属性逐渐增强.
| 实验步骤 | 实验现象 |
| 1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色. |
| 2.向新制得的Na2S溶液中滴加少量新制的氯水 | B.有气体产生,溶液变成浅红色 |
| 3.将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| 4.将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| 5.将铝条投入稀盐酸中 | E.生成淡黄色沉淀 |
(1)实验目的:探究同一周期主族元素性质的递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液等.仪器:①烧杯,②试管,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
| 实验内容 | 实验现象 | 离子方程式 |
| 1 | ||
| 2 | ||
| 3 | ||
| 4 | ||
| 5 |
(5)实验结论:同周期元素随原子序数增大,元素金属性逐渐减弱,非金属性逐渐增强.
10.氯碱工业中,与铁丝网连接的是电源的( )
| A. | 负极 | B. | 正极 | C. | 阴极 | D. | 阳极 |