题目内容
12.请写出下列反应方程式(1)对甲苯酚与足量的浓溴水反应
 +2Br2→
+2Br2→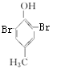 +2HBr
+2HBr(2)乙二醛与足量的新制银氨溶液反应

(3)纤维素与足量的硝酸反应制备硝化纤维
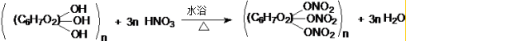 .
.
分析 (1)苯酚中邻位和对位上的H原子比较活泼,能与溴水发生取代反应,据此书写;
(2)乙二醛分子中含有2个-CHO,1mol乙二醛与4mol氢氧化二氨合银反应生成1mol乙二酸铵、4mol银、6mol氨气与2mol水;
(3)纤维素的结构单元中有3个羟基,能够与硝酸发生反应生成酯-硝酸纤维和水,发生的是酯化反应,据此完成本题.
解答 解:(1)苯酚中邻位和对位上的H原子比较活泼,能与溴水发生取代反应,对甲基苯酚中剩余邻位,对位被甲基取代,故只能与2mol溴反应,方程式为: +2Br2→
+2Br2→ +2HBr,故答案为:
+2HBr,故答案为: +2Br2→
+2Br2→ +2HBr;
+2HBr;
(2)乙二醛分子中含有2个-CHO,1mol乙二醛与4mol氢氧化二氨合银反应生成1mol乙二酸铵、4mol银、6mol氨气与2mol水,反应方程式为 ,故答案为:
,故答案为: ;
;
(3)在一定条件下,纤维素与浓H2SO4和浓HNO3的混合酸反应生成硝酸纤维和水,生成的硝酸纤维中含有酯基,该反应为酯化反应,方程式为: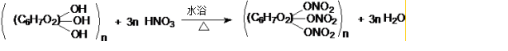 ,故答案为:
,故答案为: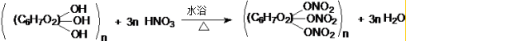 .
.
点评 本题主要考查的是有机化学反应方程式的书写,掌握酯化反应以及醛类的氧化反应是关键,难度不大.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
3.下面有关氨气的实验原理的分析中,不正确的是( )
| A. | 氨气的还原性可以解释氨气与氯化氢的反应实验 | |
| B. | NH3•H2O的热不稳定性可以解释实验室中可采用加热氨水的方法制取氨气 | |
| C. | 检验铵盐的方法是将待检物取出少量放在试管中,加苛性钠溶液,加热,用湿润红色石蕊试纸在试管口检验是否产生氨气 | |
| D. | 氨气极易溶解于水的性质可以解释氨气的喷泉实验 |
20.下列各组离子,在所给条件下一定能够大量共存的是( )
| A. | 常温下pH=7的溶液中:Fe3+、Mg2+、NO3-、SO42- | |
| B. | 常温下$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-10的溶液中:Ca2+、Mg2+、ClO-、I- | |
| C. | 在含有大量HCO3-的溶液中:K+、Na+、AlO2-、Br- | |
| D. | 加入苯酚显紫色的溶液中:Na+、Mg2+、Cl-、SO42- |
7.在N2+3H2 $?_{高温高压}^{催化剂}$ 2NH3的反应中,在5s中NH3的浓度变化了8mol/L.则NH3的平均反应速率( )
| A. | 2.4 mol/(L•s) | B. | 0.8mol/(L•s) | C. | 1.6 mol/(L•s) | D. | 0.08 mol/(L•s) |
17.有机化合物没食子茶素(EGC)结构简式如图所示.下列关于EGC的叙述中正确的是( )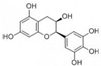

| A. | 分子中所有的原子共面 | |
| B. | 1mol EGC与4mol NaOH恰好完全反应 | |
| C. | 易发生氧化反应和取代反应,一定条件下可发生加成反应 | |
| D. | 易发生水解反应和显色反应,一定条件下可发生消去反应 |
4.下列有关表述正确的是( )
①元素所在的主族序数与最外层电子数之比为1的元素都是金属元素
②活泼金属与活泼非金属一定形成离子键
③同主族元素形成单质的熔沸点从上到下不一定都逐渐升高
④第三周期元素原子形成的简单离子半径从左到右依次减小.
①元素所在的主族序数与最外层电子数之比为1的元素都是金属元素
②活泼金属与活泼非金属一定形成离子键
③同主族元素形成单质的熔沸点从上到下不一定都逐渐升高
④第三周期元素原子形成的简单离子半径从左到右依次减小.
| A. | ①② | B. | ①③ | C. | ②④ | D. | ③ |
1.如图是电解CuCl2溶液的装置,其中c、d为石墨电极.下列说法正确的是( )


| A. | c为正极、d为负极 | |
| B. | 电路中电子的流动方向:b-d-CuCl2溶液-c-a | |
| C. | 电解过程中,d电极质量增加 | |
| D. | 电解过程中,氯离子浓度不变 |
2.下列有关概念或原理的叙述正确的是 ( )
| A. | 氨基酸、蛋白质和氧化铝一样既能与酸反应,又能与碱反应,所以它们都是两性氧化物 | |
| B. | 制造婴儿用的一次性纸尿片采用的吸水保水的材料可以是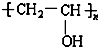 | |
| C. | 乙烯和聚乙烯都能使酸性KMnO4溶液褪色 | |
| D. | 甲酸乙酯、葡萄糖、麦芽糖、淀粉这四种物质的共同性质是,它们既可以发生水解反应,又可以发生银镜反应 |
