题目内容
7.在N2+3H2 $?_{高温高压}^{催化剂}$ 2NH3的反应中,在5s中NH3的浓度变化了8mol/L.则NH3的平均反应速率( )| A. | 2.4 mol/(L•s) | B. | 0.8mol/(L•s) | C. | 1.6 mol/(L•s) | D. | 0.08 mol/(L•s) |
分析 化学反应速率是单位时间内物质浓度的变化表示反应速率,结合V=$\frac{△c}{△t}$计算.
解答 解:在5s中NH3的浓度变化了8mol/L.则NH3的平均反应速率V(NH3)=$\frac{8mol/L}{5s}$=1.6mol/(L•s),
故选C.
点评 本题考查了化学反应速率的概念分析应用,注意概念的理解和计算得到速率单位的应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
15.在一密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)?Νι(ΧΟ)4(g),已知该反应在25℃和80℃时的平衡常数分别为5×104和2.下列说法正确的是( )
| A. | 恒温恒容下,向容器中再充入少量Ni(CO)4(g),达新平衡时,Ni(CO)4百分含量将增大 | |
| B. | 在80℃时,测得某时刻Ni(CO)4、CO浓度均为0.5 mol•L-1,则此时v(正)<v(逆) | |
| C. | 恒温恒压下,向容器中再充入少量的Ar,上述平衡将正向移动 | |
| D. | 上述生成Ni(CO)4(g)的反应为吸热反应 |
2.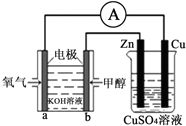 能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一.利用甲醇燃料电池设计如图所示的装置,则下列说法中不正确的是( )
能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一.利用甲醇燃料电池设计如图所示的装置,则下列说法中不正确的是( )
 能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一.利用甲醇燃料电池设计如图所示的装置,则下列说法中不正确的是( )
能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一.利用甲醇燃料电池设计如图所示的装置,则下列说法中不正确的是( )| A. | 该装置中Cu极为阳极 | |
| B. | 该装置中右池为电镀池,电解过程中CuSO4溶液pH不变 | |
| C. | b极的电极反应式为CH3OH+8OH--6e-═CO32-+6H2O | |
| D. | 当铜片的质量变化为12.8g时,a极上消耗的O2在标准状况下的体积为1.12L |
19.下列三种有机物是某些药物中的有效成分.以下说法正确的是( )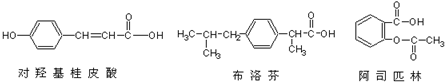

| A. | 三种有机物都能与浓溴水发生反应 | |
| B. | 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种 | |
| C. | 将1mol 的三种物质加入氢氧化钠溶液中,阿司匹林消耗氢氧化钠最多 | |
| D. | 使用FeCl3溶液和稀硫酸不能鉴别出这三种有机物 |
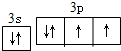
17.下表是部分短周期元素的原子半径及主要化合价,以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径 | 0.160nm | 0.143nm | 0.112nm | 0.104nm | 0.066nm |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 气态氢化物的还原性为H2T>H2R | B. | L2+与R2-的核外电子数相等 | ||
| C. | M与T形成的化合物不具有两性 | D. | 单质与稀盐酸反应的速率为L<Q |
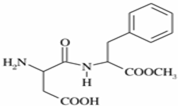 阿斯巴甜(APM)是一种甜度高、味美而热量低的甜味剂,其结构简式如图所示.
阿斯巴甜(APM)是一种甜度高、味美而热量低的甜味剂,其结构简式如图所示.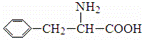 是合成APM的原料之一.苯丙氨酸的一种合成途径如图所示:
是合成APM的原料之一.苯丙氨酸的一种合成途径如图所示: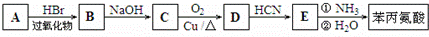


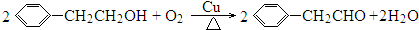
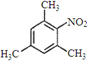 .
.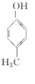 +2Br2→
+2Br2→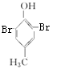 +2HBr
+2HBr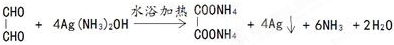
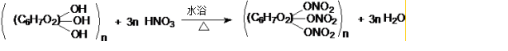 .
. .
.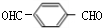 +2H2O.
+2H2O.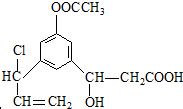 发生反应为①②③④⑤⑥
发生反应为①②③④⑤⑥