题目内容
5.铬是水体的主要的污染物之一,可以导致水生生物死亡.化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该有害物质.例如处理铬的实验循环示意图如下:(l)在如图所示的编号步骤中,其中反应①所用的试剂是硫酸酸化
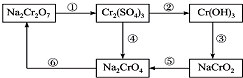 的H202,请与出该反应的离子方程式Cr2O72-+8H++3H2O2═2Cr3++3O2↑+7H2O
的H202,请与出该反应的离子方程式Cr2O72-+8H++3H2O2═2Cr3++3O2↑+7H2O(2)现有含Cr3+和Fe3+的溶液,使用NaOH溶液和盐酸,可将这两种离子相互分离,根据如图信息分析,在涉及的过滤操作中,上述两种离子的存在形态分别是CrO2-、Fe(OH)3.(写化学式)
(3)铬的化合价除了示意图中涉及的+3和+6外,还有0、+2、+4和+5等.现有24mL浓度为0.05mol/L的Na2S03溶液恰好与20mL浓度为0.02mol/L的Na2Cr207溶液完全反应.己知Na2S04被Na2Cr207氧化为Na2S04,则元素Cr在还原产物中的化合价为+3.
(4)步骤⑤应该加入氧化剂剂(填“还原”或“氧化”).
分析 (1)H2O2既具有氧化性,又具有还原性;Cr2O72-具有强氧化性,能将H2O2氧化为O2,反应中+6价Cr元素被还原为+3价;
(2)从反应③可以看出,Cr(OH)3可以与NaOH溶液反应生成NaCrO2,所以除去Fe3+中的Cr3+时,可以加入过量的NaOH溶液,使Cr3+转化为CrO,Fe3+转化为Fe(OH)3沉淀,在过滤得到的Fe(OH)3中加入盐酸即得到FeCl3溶液;
(3)Na2SO3被氧化为Na2SO4,S元素化合价由+4价升高为+6价;Na2Cr2O7中Cr元素发生还原反应,令Cr元素在产物中的化合价为a价,根据电子转移守恒计算a的值;
(4)Cr元素的化合价从+3升高到了+6价,Cr元素被氧化.
解答 解:(1)H2O2既具有氧化性,又具有还原性;Cr2O72-具有强氧化性,能将H2O2氧化为O2,反应中+6价Cr元素被还原为+3价,离子反应为Cr2O72-+8H++3H2O2═2Cr3++3O2↑+7H2O,故答案为:Cr2O72-+8H++3H2O2═2Cr3++3O2↑+7H2O;
(2)从反应③可以看出,Cr(OH)3可以与NaOH溶液反应生成NaCrO2,所以除去Fe3+中的Cr3+时,可以加入过量的NaOH溶液,使Cr3+转化为CrO,Fe3+转化为Fe(OH)3沉淀,在过滤得到的Fe(OH)3中加入盐酸即得到FeCl3溶液,故答案为:CrO2-;Fe(OH)3;
(3)令Cr元素在产物中的化合价为a价,根据电子转移守恒,则:24×10-3L×0.05mol/L×(6-4)=20×10-3L×0.02mol/L×2×(6-a),解得a=+3,
故答案为:+3;
(4)步骤⑤中,Cr元素的化合价从+3升高到了+6价,所以需要加入氧化剂,故答案为:氧化剂.
点评 本题考查氧化还原反应及计算,为高频考点,把握发反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意(3)中电子守恒应用,题目难度不大.

| A. | 将少量金属钠放入冷水中:Na+2H2O=Na++2OH-+H2↑ | |
| B. | 将铝片加入盐酸溶液中:2Al+6H+=2Al3++3H2↑ | |
| C. | 向碳酸钠溶液中加入CH3COOH:CO${\;}_{3}^{2-}$+2H+=CO2↑+H2O | |
| D. | 向澄清石灰水中通入过量的二氧化碳:Ca2++2OH-=CaCO3↓+H2O |
| A. | 前2 s,以N2O4的浓度表示的平均反应速率为 0.01 mol•L-1•s-1 | |
| B. | 在2 s时体系内的压强为开始时的1.1倍 | |
| C. | 在平衡时体系内含N2O40.25 mol | |
| D. | 平衡时,如果压缩容器容积,则可提高N2O4的转化率 |
| A. | Mg2+、NH4+、SO42-、Cl- | B. | Cu2+、Na+、HCO3-、OH- | ||
| C. | K+、Ca2+、NO3-、CO32- | D. | Ag+、Fe3+、Cl-、NO3- |
 某混合溶液中,一定含有Cl-、Br-、I-,可能含有的离子如下表所示.
某混合溶液中,一定含有Cl-、Br-、I-,可能含有的离子如下表所示.| 可能大量含有的阳离子 | H+、Ag+、Mg2+、Al3+、NH4+、Fe3+ |
| 可能大量含有的阴离子 | CO32-、AlO2-、NO3- |
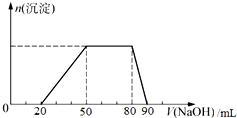
探究一:取10mL该混合溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如图所示.
探究二:取1L该混合溶液,向该溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如下表所示.
| Cl2的体积(标准状况) | 5.6L | 11.2L | 22.4L |
| n(Cl-) | 2.5mol | 3.0mol | 4.0mol |
| n(Br-) | 3.0mol | 2.8mol | 1.8mol |
| n(I-) | X mol | 0 | 0 |
| A. | X=0.3 | |
| B. | 溶液中n(Cl-):n(Br-):n(I-)=10:15:4 | |
| C. | 加入的氢氧化钠溶液的浓度为1.45mol•L-1 | |
| D. | 溶液中大量存在的离子共有六种 |
| A. | 1摩尔任何物质都含有6.02×1023个分子 | |
| B. | 摩尔是国际单位制中7个基本物理量之一 | |
| C. | 含有6.02×1023个氧原子的H3PO4的物质的量是0.25mol | |
| D. | 氧气的摩尔质量等于它的相对原子质量 |
| A. | NaAlO2 | B. | KAl(SO4)2•12H2O | C. | Al(OH)3 | D. | Al2O3 |
| A. | 根据气体的相对分子质量,可以比较相同状况下气体密度的大小 | |
| B. | 根据甲烷和乙烷的熔点,可以比较二者晶体中的分子间作用力的大小 | |
| C. | 比较同周期金属元素原子半径的大小,可以推断元素的金属性强弱 | |
| D. | 根据液体密度的大小,可以判断液体的挥发性的强弱 |