题目内容
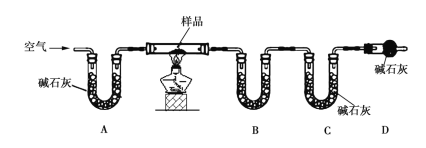
【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,可用于处理部分含硫废水。某小组在实验室中利用下列装置制备ClO2(此制备方法中经空气稀释的SO2与ClO2不反应)。
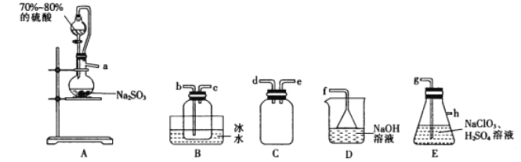
回答下列问题:
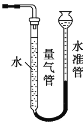
(1)仪器X的名称是________。
(2)欲选择上图中的装置收集ClO2,其连接顺序为a→_________________________(按气流方向,用小写字母表示)。
(3)装置C的作用是_________,装置E中反应的离子方程式为________________________。
(4)处理含硫(Na2S)碱性废水时,ClO2与Na2S反应(S2-被氧化为SO42-)的离子方程式为__________;处理含硫碱性废水时,相同条件下同体积的ClO2相对于Cl2的优点是__________________________。
(5)ClO2很不稳定,需现用现配,为测定所得溶液中ClO2的含量,进行下列实验:
步骤1:准确量取V1 mL ClO2溶液加入锥形瓶中。
步骤2:用稀硫酸调节ClO2溶液的pH≤2.0,再加入足量KI晶体,静置片刻。
步骤3:加入指示剂,用c mol·L-1的Na2S2O3标准溶液滴定至终点时,消耗V2 mL Na2S2O3标准溶液。
(已知:2ClO2+8H++10I-===2C1-+5I2+4H2O;2S2O32-+I2===2I-+S4O62-)
①配制100mL c mol·L-1 Na2S2O3标准溶液时,用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管和______。
②原溶液中ClO2的含量为____________(用含c、V1、V2的代数式表示)g·L-1。
【答案】分液漏斗 d→e→g→h→b→c→f 防倒吸 SO2 +2ClO3 = 2ClO2 +SO42 8ClO2 + 5S2 + 4H2O=8Cl + 5SO42 + 8H+; ClO2除硫效果更好,ClO2在水中的溶解度大、剩余的ClO2不会产生二次污染、均被还原为氯离子时,ClO2得到的电子数是氯气的2.5倍; 100mL容量瓶 ![]() g/L
g/L
【解析】
(1)根据仪器的构造及用途作答;
(2)装置A中亚硫酸钠与浓硫酸发生反应制备二氧化硫气体,在装置E中发生生成二氧化氯的反应,为防止倒吸,A与E之间连接装置C,二氧化氯沸点较低,故在B中冰水浴收集,最后用D装置中的氢氧化钠吸收未反应完的二氧化硫,防止污染空气,据此分析解答;
(3)装置C为安全瓶,根据其用途作答;装置E中发生氧化还原反应,根据电子转移数守恒配平该反应;
(4)ClO2具有强氧化性,与Na2S发生氧化还原反应;结合ClO2在水中的溶解度比氯气大,且除硫效果彻底、产物无污染等角度分析作答;
(5)①根据配制100 ml c molL-1Na2S2O3标准溶液的实验操作步骤分析所缺玻璃仪器;
②由反应可得关系式:2ClO2~5I2~10S2O32-,根据关系式计算ClO2的物质的量浓度,进而计算其含量;
(1)仪器X与橡皮管连接,平衡内外气压,便于液体顺利留下,该仪器的名称是分液漏斗,
故答案为:分液漏斗;
(2)二氧化硫从a进入装置E中反应,为防止倒吸,故应在之前有安全瓶,则a→d→e,再连接E装置中的g,二氧化氯沸点较低,故在B中冰水浴收集,为充分冷却,便于收集,故连接b,最后用氢氧化钠吸收未反应完的二氧化硫,防止污染空气,连接顺序为:a→d→e→g→h→b→c→f;
故答案为:d→e→g→h→b→c→f;
(3)二氧化硫从a若进入装置E中反应,可能会倒吸,故再A与E之间安装C装置,其作用是防止倒吸,而E为发生装置,其中二氧化硫与NaClO3反应的离子方程式为:SO2 +2ClO3 = 2ClO2 +SO42,
故答案为:防倒吸;SO2 +2ClO3 = 2ClO2 +SO42;
(4)S2-被氧化为SO42-,ClO2会被还原为稳定的Cl,根据氧化还原反应中得失电子数守恒可知,该离子方程式为:8ClO2 + 5S2 + 4H2O=8Cl + 5SO42 + 8H+;与氯气相比,ClO2除硫效果彻底,氧化产物硫酸根更稳定、ClO2在水中的溶解度大、剩余的ClO2不会产生二次污染、均被还原为氯离子时,ClO2得到的电子数是氯气的2.5倍;
故答案为:8ClO2 + 5S2 + 4H2O=8Cl + 5SO42 + 8H+;ClO2除硫效果更好,ClO2在水中的溶解度大、剩余的ClO2不会产生二次污染、均被还原为氯离子时,ClO2得到的电子数是氯气的2.5倍。
(5)①称量后在烧杯中溶解,并用玻璃棒搅拌,移入100 mL容量瓶中,加水至距离容量瓶刻度线12 cm处改用胶头滴管定容,
故答案为:100mL容量瓶;
②由反应可得关系式:2ClO2~5I2~10S2O32-,可知V1 mL×c(ClO2):V2mL×c(Na2S2O3)=2:10,则c(ClO2) = ![]() mol/L,则其含量为
mol/L,则其含量为![]() mol/L×67.5 g/mol =
mol/L×67.5 g/mol = ![]() g/L,
g/L,
故答案为:![]() g/L。
g/L。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案