题目内容
列关于同主族元素的说法错误的是( )
| A、同主族元素随原子序数递增,元素原子的得电子能力逐渐增强 |
| B、同主族元素随原子序数递增,单质氧化能力逐渐减弱 |
| C、同主族元素原子最外层电子数都相同 |
| D、同主族元素的原子半径,随原子序数增大而逐渐增大 |
考点:同一主族内元素性质递变规律与原子结构的关系
专题:元素周期律与元素周期表专题
分析:A.同主族元素随原子序数递增,元素原子的得电子能力逐渐减弱;
B.同主族元素随原子序数递增,单质氧化能力逐渐减弱;
C.同主族元素原子最外层电子数都相同,与其族序数相等;
D.同主族元素的原子半径,随原子序数增大而逐渐增大.
B.同主族元素随原子序数递增,单质氧化能力逐渐减弱;
C.同主族元素原子最外层电子数都相同,与其族序数相等;
D.同主族元素的原子半径,随原子序数增大而逐渐增大.
解答:
解:A.同主族元素随原子序数递增,原子半径逐渐增大,原子核对最外层电子的吸引力逐渐减小,则元素原子的得电子能力逐渐减弱,故A错误;
B.同主族元素随原子序数递增,原子半径逐渐增大,原子核对最外层电子的吸引力逐渐减小,则元素原子的得电子能力逐渐减弱,导致单质氧化能力逐渐减弱,故B正确;
C.同主族元素原子最外层电子数都相同,与其族序数相等,其化学性质相似,故C正确;
D.同主族元素随原子序数递增,原子核对最外层电子的吸引力逐渐减小,导致原子半径增大,故D正确;
故选A.
B.同主族元素随原子序数递增,原子半径逐渐增大,原子核对最外层电子的吸引力逐渐减小,则元素原子的得电子能力逐渐减弱,导致单质氧化能力逐渐减弱,故B正确;
C.同主族元素原子最外层电子数都相同,与其族序数相等,其化学性质相似,故C正确;
D.同主族元素随原子序数递增,原子核对最外层电子的吸引力逐渐减小,导致原子半径增大,故D正确;
故选A.
点评:本题考查了同一主族元素性质的递变规律,根据同一主族元素最外层电子排布特点、元素周期律等知识点来分析解答,题目难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
 常温下,用0.1mol/L NaOH溶液滴定20mL 0.1mol/L CH3COOH溶液的滴定曲线如图.下列说法错误的是( )
常温下,用0.1mol/L NaOH溶液滴定20mL 0.1mol/L CH3COOH溶液的滴定曲线如图.下列说法错误的是( )| A、点①所示溶液中:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | ||
| B、点②所示溶液中:c(CH3COOH)>c(Na+)=c(CH3COO-)>c(H+)=c(OH-) | ||
| C、点③所示溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH-) | ||
D、在整个滴定过程中:溶液中
|
下列叙述不正确的是( )
| A、金属X能与NaOH溶液反应放出H2,但金属Y不能,则Y的金属性一定比X弱 |
| B、在合成氨反应达到平衡时,只增加N2的物质的量,达新平衡后N2的百分含量增大 |
| C、在铁件上镀铜时,铁和电源负极相连,铜和正极相连,电解质溶液是CuSO4溶液 |
| D、Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化 |
欧盟正考虑在欧盟范围内全面禁止使用塑料袋.下列有关说法正确的是( )
| A、塑料垃圾可直接露天焚烧 |
| B、实施“禁塑令”有助于遏制白色污染 |
| C、纤维素、油脂、蛋白质均属于有机高分子 |
D、聚丙烯结构式为: |
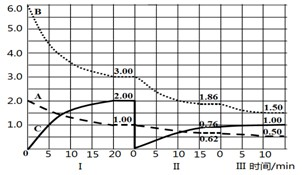 反应aA(g)+bB(g)?cC(g)(△H<0)在等容条件下进行.改变其它反应条件,在I、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示,下列说法不正确的是( )
反应aA(g)+bB(g)?cC(g)(△H<0)在等容条件下进行.改变其它反应条件,在I、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示,下列说法不正确的是( )| A、反应的化学方程式中,a:b:c=1:3:2 |
| B、A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A),最大的是vⅠ(A) |
| C、第Ⅱ阶段反应温度小于第Ⅲ阶段反应温度 |
| D、由第一次平衡到第二次平衡,采取的措施是从反应体系中移走C |
下列指定物质的个数比不为1:1的是( )
| A、D2O中质子数与中子数 |
| B、Na2O2中的阴,阳离子数 |
| C、SO2与氯水反应生成两种强酸的反应中,氧化剂与还原剂 |
| D、沸水时纯水中H+与OH- |
下列离子方程式正确的是( )
| A、SiO2与NaOH溶液:SiO2+2Na++2OH-═Na2SiO3↓+H2O |
| B、将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-═SO32-+2HClO |
| C、向含有0.4mol FeBr2的溶液中通入0.1mol Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
| D、NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |