题目内容
下列指定物质的个数比不为1:1的是( )
| A、D2O中质子数与中子数 |
| B、Na2O2中的阴,阳离子数 |
| C、SO2与氯水反应生成两种强酸的反应中,氧化剂与还原剂 |
| D、沸水时纯水中H+与OH- |
考点:质量数与质子数、中子数之间的相互关系,离子晶体,水的电离,二氧化硫的化学性质
专题:原子组成与结构专题
分析:A.D中质子数为1,中子数为1;O中质子数为8,中子数为8;
B.Na2O2 是由2个钠离子与过氧根离子通过离子键构成;
C.SO2与氯水反应的化学方程式Cl2+SO2+2H2O=2HCl+H2SO4,据此解答;
D.水的电离方程式为:H2O?H++OH-,据此解答.
B.Na2O2 是由2个钠离子与过氧根离子通过离子键构成;
C.SO2与氯水反应的化学方程式Cl2+SO2+2H2O=2HCl+H2SO4,据此解答;
D.水的电离方程式为:H2O?H++OH-,据此解答.
解答:
解:A.D2O中质子数是10,中子数是10,故A正确;
B.1个Na2O2中含1个O22-离子,2个钠离子,阳离子数:阴离子数为2:1,故B错误;
C.SO2与氯水反应的化学方程式Cl2+SO2+2H2O=2HCl+H2SO4,二氧化硫中的硫元素化合价升高为还原剂,氯气中氯元素化合价降低为氧化剂,二者物质的量之比为1:1,故C正确;
D.水的电离方程式为:H2O?H++OH-,所以水电离产生的氢离子与氢氧根离子之比为1:1,故D正确;
故选:B.
B.1个Na2O2中含1个O22-离子,2个钠离子,阳离子数:阴离子数为2:1,故B错误;
C.SO2与氯水反应的化学方程式Cl2+SO2+2H2O=2HCl+H2SO4,二氧化硫中的硫元素化合价升高为还原剂,氯气中氯元素化合价降低为氧化剂,二者物质的量之比为1:1,故C正确;
D.水的电离方程式为:H2O?H++OH-,所以水电离产生的氢离子与氢氧根离子之比为1:1,故D正确;
故选:B.
点评:本题考查了不同微粒数之间的关系,题目难度不大,明确物质的结构和性质是解题关键,注意过氧化钠的构成.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
化学与环境、材料、能源关系密切,下列说法错误的是( )
| A、合成纤维、塑料、合成橡胶都是高分子化合物 |
| B、煤的气化和煤的液化都可以使煤变为清洁能源,煤的气化和煤的液化都属于物理变化 |
| C、我国首艘航母“辽宁舰”上用于舰载机降落的拦阻索是特种钢缆,属于金属材料 |
| D、页岩气是从页岩层中开采出来的天然气.由于产气的页岩分布广、厚度大,且普遍含气,故可以成为新的化石燃料来源 |
25℃时,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
| A、将0.2mol/L的某一元酸HA溶液和0.1mol/L NaOH溶液等体积混合后,混合液pH大于7,则反应后的混合液:2c(OH-)+c(A-)=2c(H+)+c(HA) |
| B、pH均为9的三种溶液:CH3COOH、Na2CO3、NaOH,其物质的量浓度的大小顺序是NaOH 溶液>CH3COOH溶液>Na2CO3溶液 |
| C、pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:c(R2-)+c(HR-)=c(Na+) |
| D、0.2mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合:c(H+)=c(OH-)+c(HCO3-)+2c(H2CO3) |
在下列变化中,只发生物理变化的是( )
| A、空气液化制取氮气 |
| B、酸雨侵蚀建筑物 |
| C、荔枝酿酒 |
| D、生石灰遇水成为熟石灰 |
列关于同主族元素的说法错误的是( )
| A、同主族元素随原子序数递增,元素原子的得电子能力逐渐增强 |
| B、同主族元素随原子序数递增,单质氧化能力逐渐减弱 |
| C、同主族元素原子最外层电子数都相同 |
| D、同主族元素的原子半径,随原子序数增大而逐渐增大 |
下列过程或事实涉及氧化还原反应的是( )
①蔗糖炭化 ②用氢氟酸雕刻玻璃 ③铁遇冷的浓硫酸钝化 ④装碱液的试剂瓶不用玻璃塞 ⑤雷雨发庄稼 ⑥实际使用的浓硝酸显黄色.
①蔗糖炭化 ②用氢氟酸雕刻玻璃 ③铁遇冷的浓硫酸钝化 ④装碱液的试剂瓶不用玻璃塞 ⑤雷雨发庄稼 ⑥实际使用的浓硝酸显黄色.
| A、①③⑤⑥ | B、②④ |
| C、②③④⑥ | D、①②③④⑤⑥ |


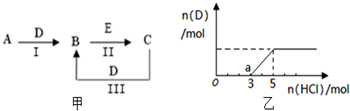 A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图甲所示
A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图甲所示