题目内容
拆开1mol H-H键、1mol N-H、1mol N≡N键需要的能量分别是436kJ、391kJ、946kJ,则1mol N2完全反应生成NH3的反应热为 ,1mol H2完全反应生成NH3所放出的热量为 .
考点:反应热和焓变
专题:化学反应中的能量变化
分析:化学反应中,化学键断裂吸收能量,形成新化学键放出能量,根据方程式计算分别吸收和放出的能量,以此计算反应热并判断吸热还是放热.
解答:
解:在反应N2+3H2?2NH3中,断裂3molH-H键,1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,生成2mol NH3,共形成6mol N-H键,放出的能量为:6×391kJ=2346kJ,吸收的能量少,放出的能量多,该反应为放热反应,放出的热量为:2346kJ-2254kJ=92kJ;
N2(g)+3H2(g)?2NH3(g)△H=-92kJ?mol-1,1mol H2完全反应生成NH3所放出的热量=
=30.7KJ;
故答案为:-92kJ?mol-1,30.7KJ;
N2(g)+3H2(g)?2NH3(g)△H=-92kJ?mol-1,1mol H2完全反应生成NH3所放出的热量=
| 92KJ |
| 3 |
故答案为:-92kJ?mol-1,30.7KJ;
点评:本题主要考查了热化学方程式的书写,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比.同时还考查了反应热的计算,题目难度不大,注意把握从键能的角度计算反应热的方法.

练习册系列答案
相关题目
列关于同主族元素的说法错误的是( )
| A、同主族元素随原子序数递增,元素原子的得电子能力逐渐增强 |
| B、同主族元素随原子序数递增,单质氧化能力逐渐减弱 |
| C、同主族元素原子最外层电子数都相同 |
| D、同主族元素的原子半径,随原子序数增大而逐渐增大 |
下列说法不正确的是( )
| A、汽车尾气中有NOx,主要是汽油不充分燃烧引起的 |
| B、发泡塑料饭盒主要材质是高分子材料,不适于盛放含油较多的食品 |
| C、BaSO4难溶于水,医疗上可用做钡餐 |
| D、为改善食物的色、香、味并防止变质,可在其中加入适量食品添加剂 |
分子式为C4H8Cl2,含有两个甲基的同分异构体共有(不考虑立体异构)( )
| A、3种 | B、5种 | C、4种 | D、6种 |

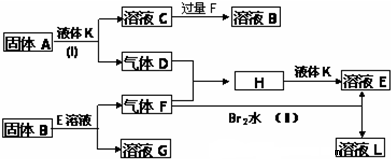
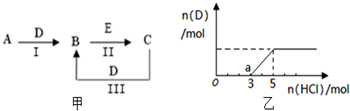 A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图甲所示
A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图甲所示