МвДҝДЪИЭ
ЎҫМвДҝЎҝProlitaneКЗТ»ЦЦҝ№ТЦУфТ©ОпЈ¬ТФ·јПгМюAОӘФӯБПөДәПіЙВ·ПЯИзПВЈә
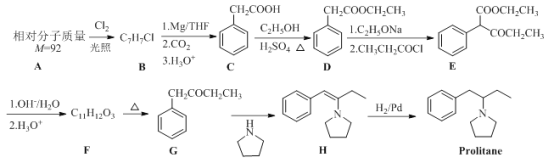
Зл»ШҙрТФПВОКМвЈә
(1)DөД»ҜС§ГыіЖОӘ______Ј¬HЎъProlitaneөД·ҙУҰАаРНОӘ______ЎЈ
(2)EөД№ЩДЬНЕГыіЖ·ЦұрОӘ______әН______ЎЈ
(3)BөДҪб№№јтКҪОӘ______ЎЈ
(4)FЎъGөД»ҜС§·ҪіМКҪОӘ______ЎЈ
(5)CөДН¬·ЦТм№№МеЦРДЬН¬КұВъЧгПВБРМхјюөД№ІУР______ЦЦ(І»ә¬БўМеТм№№)Ј»
ўЩКфУЪ·јПг»ҜәПОп ўЪДЬ·ўЙъТшҫө·ҙУҰ ўЫДЬ·ўЙъЛ®Ҫв·ҙУҰ
ЖдЦРәЛҙЕ№ІХсЗвЖЧПФКҫОӘ4Чй·еЈ¬Жд·еГж»эұИОӘ3ЎГ2ЎГ2ЎГ1Ј¬Рҙіц·ыәПТӘЗуөДёГН¬·ЦТм№№МеөДҪб№№јтКҪ______ЎЈ
(6)ІОХХProlitaneөДәПіЙВ·ПЯЈ¬ЙијЖТ»МхУЙұҪәНТТҙјОӘФӯБПЦЖұёұҪјЧЛбТТхҘөДәПіЙВ·ПЯ_____________(ЖдЛыОЮ»ъКФјБәНИЬјБИОСЎ)ЎЈ
Ўҫҙр°ёЎҝұҪТТЛбТТхҘ јУіЙ·ҙУҰ»т»№Фӯ·ҙУҰ фК»щ хҘ»щ ![]()
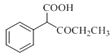
![]()
![]() + CO2Ўь ЎҫҙрМвҝХ7Ўҝ4
+ CO2Ўь ЎҫҙрМвҝХ7Ўҝ4 ![]()
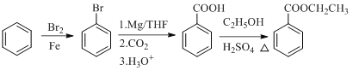
ЎҫҪвОцЎҝ
(1)ёщҫЭDөДҪб№№јтКҪҝЙЦӘDөДГыіЖОӘұҪТТЛбТТхҘЈ»H 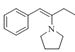 УлЗвЖшФЪҙЯ»ҜјБҙжФЪПВ·ўЙъјУіЙ·ҙУҰІъЙъProlitane
УлЗвЖшФЪҙЯ»ҜјБҙжФЪПВ·ўЙъјУіЙ·ҙУҰІъЙъProlitane![]() Ј¬УлЗвЖшөДјУіЙ·ҙУҰТІҪР»№Фӯ·ҙУҰЈ»
Ј¬УлЗвЖшөДјУіЙ·ҙУҰТІҪР»№Фӯ·ҙУҰЈ»
(2)EҪб№№јтКҪОӘ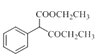 Ј¬ёщҫЭҪб№№јтКҪҝЙЦӘә¬УРөД№ЩДЬНЕ·ЦұрОӘхҘ»щәНфК»щЈ»
Ј¬ёщҫЭҪб№№јтКҪҝЙЦӘә¬УРөД№ЩДЬНЕ·ЦұрОӘхҘ»щәНфК»щЈ»
(3)AПа¶Ф·ЦЧУЦКБҝКЗ92Ј¬ҝЙТФУлВИЖшФЪ№вХХМхјюПВ·ўЙъИЎҙъ·ҙУҰІъЙъC7H7ClЈ¬ФтAКЗјЧұҪ![]() Ј¬BКЗ
Ј¬BКЗ![]() Ј»
Ј»
(4)E( 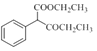 )ФЪјоРФМхјюПВ·ўЙъЛ®Ҫв·ҙУҰЈ¬И»әуЛб»ҜөГөҪFЈә
)ФЪјоРФМхјюПВ·ўЙъЛ®Ҫв·ҙУҰЈ¬И»әуЛб»ҜөГөҪFЈә Ј¬ёГОпЦКјУИИ·ўЙъНСфИ·ҙУҰІъЙъCO2әН
Ј¬ёГОпЦКјУИИ·ўЙъНСфИ·ҙУҰІъЙъCO2әН![]() Ј¬·ҙУҰөД·ҪіМКҪОӘЈә
Ј¬·ҙУҰөД·ҪіМКҪОӘЈә
![]()
![]() + CO2ЎьЈ»
+ CO2ЎьЈ»
(5)CҪб№№јтКҪОӘ![]() Ј¬ЖдН¬·ЦТм№№МеТӘЗуўЩКфУЪ·јПг»ҜәПОпЈ¬ЛөГчә¬УРұҪ»·Ј»ўЪДЬ·ўЙъТшҫө·ҙУҰЈ¬ЛөГчә¬УРИ©»щЈ¬ўЫДЬ·ўЙъЛ®Ҫв·ҙУҰЈ¬ЛөГчә¬УРхҘ»щЈ¬ФтЖдОӘјЧЛбРОіЙөДхҘЈ¬ҝЙДЬҪб№№ОӘ
Ј¬ЖдН¬·ЦТм№№МеТӘЗуўЩКфУЪ·јПг»ҜәПОпЈ¬ЛөГчә¬УРұҪ»·Ј»ўЪДЬ·ўЙъТшҫө·ҙУҰЈ¬ЛөГчә¬УРИ©»щЈ¬ўЫДЬ·ўЙъЛ®Ҫв·ҙУҰЈ¬ЛөГчә¬УРхҘ»щЈ¬ФтЖдОӘјЧЛбРОіЙөДхҘЈ¬ҝЙДЬҪб№№ОӘ![]() Ўў
Ўў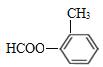 Ўў
Ўў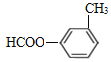 Ўў
Ўў![]() Ј¬№ІУР4ЦЦЈ»ЖдЦРәЛҙЕ№ІХсЗвЖЧПФКҫОӘ4Чй·еЈ¬Жд·еГж»эұИОӘ3ЎГ2ЎГ2ЎГ1Ј¬·ыәПТӘЗуөДёГН¬·ЦТм№№МеөДҪб№№јтКҪОӘ
Ј¬№ІУР4ЦЦЈ»ЖдЦРәЛҙЕ№ІХсЗвЖЧПФКҫОӘ4Чй·еЈ¬Жд·еГж»эұИОӘ3ЎГ2ЎГ2ЎГ1Ј¬·ыәПТӘЗуөДёГН¬·ЦТм№№МеөДҪб№№јтКҪОӘ![]() Ј»
Ј»
(6)УЙұҪәНТТҙјОӘФӯБПЦЖұёұҪјЧЛбТТхҘөДәПіЙВ·ПЯКЗ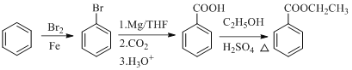 ЎЈ
ЎЈ

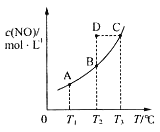
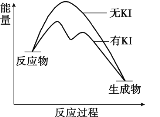
ЎҫМвДҝЎҝПт20 mL 0.40 mol/L H2O2ИЬТәЦРјУИлЙЩБҝKIИЬТәЈәўЎЈ®H2O2+I-=H2O+IO©ҒЈ»ўўЈ®H2O2+IO©Ғ= H2O+O2Ўь+ I©ҒЎЈH2O2·ЦҪв·ҙУҰ№эіМЦРДЬБҝұд»ҜәНІ»Н¬КұҝМІвөГЙъіЙO2өДМе»э(ТСХЫЛгұкЧјЧҙҝц)ИзПВЎЈ
t/min | 0 | 5 | 10 | 15 | 20 |
V(O2)/mL | 0.0 | 12.6 | 20.16 | 28.0 | 32.7 |
ПВБРЕР¶ПІ»ХэИ·өДКЗ
A. ҙУНјЦРҝЙТФҝҙіцЈ¬KIДЬФцҙуH2O2өД·ЦҪвЛЩВК
B. ·ҙУҰўЎКЗ·ЕИИ·ҙУҰЈ¬·ҙУҰўўКЗОьИИ·ҙУҰ
C. 0~10 minөДЖҪҫщ·ҙУҰЛЩВКЈәv(H2O2)ЎЦ9.0ЎБ10-3 mol/(LЎӨmin)
D. H2O2ФЪ·ҙУҰ№эіМЦРјИМеПЦБЛСх»ҜРФЈ¬УЦМеПЦБЛ»№ФӯРФ
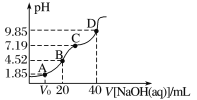
ЎҫМвДҝЎҝ(1)ТСЦӘіЈОВКұЈ¬0.1mol/LҙЧЛбФЪЛ®ЦРУР0.1%·ўЙъөзАлЈ¬ФтёГИЬТәөДpH=_____Ј¬ҙЧЛбөДөзАлЖҪәвіЈКэKa=______ЎЈ
(2)ПтұщҙЧЛбЦРЦрөОјУЛ®Ј¬ИЬТәөјөзРФЛжјУИлЛ®өДМе»эұд»ҜИзНјЛщКҫЈә
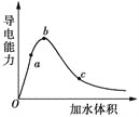
ўЩaЎўbЎўcИэөгИЬТәЦРCH3COOHөДөзАліМ¶ИУЙҙуөҪРЎөДЛіРтКЗ___ЎЈ
ўЪaЎўcБҪөг¶ФУҰөДИЬТә·ЦұрОьКХ°ұЖшЈ¬ИфБҪИЬТәЧоЦХpHҫщОӘ7ЈЁ25ЎжКұЈ©Ј¬ФтaөгИЬТәЦРөДc(CH3COO-)_______cөгИЬТәЦРөДc(NH4+)ЎЈ(МоЎ°<ЎұЎўЎ°>Ўұ»тЎ°=Ўұ)
(3)25ЎжКұЈ¬Іҝ·ЦОпЦКөДөзАлЖҪәвіЈКэИзұнЛщКҫЈә
»ҜС§КҪ | CH3COOH | NH3ЎӨH2O | H2CO3 | HCN |
өзАлЖҪәвіЈКэ | 1.7ЎБ10-5 | 1.7ЎБ10-5 | K1=4.3ЎБ10-7 K2=5.6ЎБ10-11 | K=5.0ЎБ10-10 |
Зл»ШҙрПВБРОКМвЈә
ўЩH2CO3өДөЪ¶юј¶өзАлЖҪәвіЈКэөДұнҙпКҪKa2=_______ЎЈ
ўЪ25ЎжКұЈ¬Пт0.1molL-1өД°ұЛ®ЦР»ә»әНЁИлCO2ЖшМеөД№эіМЦР(әцВФИЬТәМе»эөДұд»Ҝ)Ј¬ПВБРұнҙпКҪөДКэЦөұдРЎөДКЗ___ЎЈ
AЈ®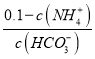 BЈ®
BЈ®![]() CЈ®
CЈ®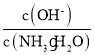 DЈ®
DЈ®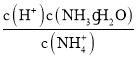
ўЫПтNaCNИЬТәЦРНЁИлЙЩБҝCO2ЖшМеЈ¬·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪОӘ___ЎЈ