题目内容
11.设NA为阿伏加德罗常数的数值,下列说法错误的是( )| A. | 一定条件下,2 mol SO2和1 mol O2混合在密闭容器中充分反应后容器中的分子数大于2NA | |
| B. | 256 g S8分子中含S-S键为7NA个.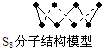 | |
| C. | 由1 mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 | |
| D. | 1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA个 |
分析 A、二氧化硫与氧气反应生成三氧化硫的反应为可逆反应,反应物只能部分转化成生成物;
B、一个S8分子中含8个S-S键,据此计算出256g晶体中含有的S-S的数目;
C、根据电荷守恒判断:溶液为中性,氢离子与氢氧根离子浓度相等,则钠离子与醋酸根离子相等;
D、钠为1价金属,1mol钠完全反应失去1mol电子
解答 解:A、2mol SO2和1mol O2混合在闭容器中加热反应后,由于该反应为体积减小的可逆反应,反应生成的三氧化硫的物质的量小于2mol,反应后气体的物质的量大于2mol,分子数大于2NA,故A正确;
B、256g S8晶体含有S8的物质的量为1mol,1molS8中含有8mol S-S键,含有的S-S键为8NA个,故B错误;
C、由1mol CH3COONa和少量CH3COOH形成的中性溶液中,含有1mol钠离子;根据电荷守恒,溶液为中性,氢离子与氢氧根离子物质的量相等,则钠离子与CH3COO-的物质的量相等,所以溶液中含有CH3COO-的物质的量为1mol,含有的CH3COO-数目为NA个,故C正确;
D、1molNa完全反应失去1mol电子,无论产物为氧化钠还是过氧化钠,转移的电子数都为1mol,转移电子总数NA个,故D正确;
故选B.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项C为易错点,注意电荷守恒的应用

练习册系列答案
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
1.下列关于分类的说法正确的是( )
| A. | 活性炭、C60、金刚砂都是碳的同素异形体 | |
| B. | Fe2O3、Na2O2、K2O都是碱性氧化物 | |
| C. | 淀粉、蛋白质、油脂都属于有机高分子化合物 | |
| D. | 纯碱、氯化铵、明矾都是盐且都属于强电解质 |
19.下列说法正确的是( )
| A. | 右列图标均与燃烧和爆炸有关 | |
| B. | 棉、麻、蚕丝、羊毛及合成纤维都属于纤维,但均不含纤维素 | |
| C. | 科学家用单个分子制成了“纳米车”,它能在人工操纵下运输药物分子到病源处释放以杀死癌细胞.“纳米车”说明在一定条件下,分子的热运动须在人工操纵下才能进行 | |
| D. | 捕获工业排放的CO2,既能降低地球的温室效应又能用来合成聚碳酸酯可降解塑料,实现碳的循环利用 |
16.甲、乙是由短周期元素组成的常见物质或微粒,在中学化学中有许多物质或微粒能满足下列相互转化关系:甲$\stackrel{H+}{→}$乙$\stackrel{OH-}{→}$甲.下列说法正确的是( )
| A. | 甲有可能是AlO2- 也有可能是Al3+ | |
| B. | 若乙为无色无味气体,则甲一定是CO32- | |
| C. | 若甲是具有刺激性气味的气体,则甲、乙具有相同的电子数 | |
| D. | 若甲、乙均为离子,甲、乙两种离子在同一溶液中一定不能大量共存 |
3.下列说法正确的是( )
| A. | 含有共价键的物质一定是共价化合物 | |
| B. | 分子中只有共价键的化合物一定是共价化合物 | |
| C. | 离子化合物中一定没有共价键 | |
| D. | 离子化合物一定含有金属元素 |
1.短周期元素R、T、X、Y、Z在元素周期表的相对位置如表所示,它们的最外层电子数之和为31.则下列判断正确的是( )
| R | T | |
| X | Y | Z |
| A. | R位于元素周期表中第二周期第ⅣA族 | |
| B. | 原子半径:X<R<T | |
| C. | 最简单气态氢化物稳定性:T>R>Y | |
| D. | 最高价氧化物的水化物酸性:T>R>Y |

 .
.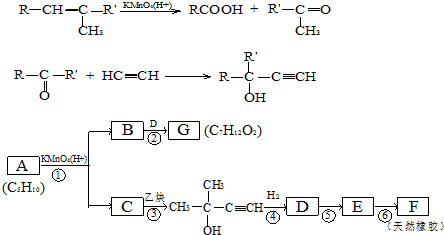
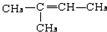 ,CCH3COCH3,ECH2=C(CH3)CH=CH2
,CCH3COCH3,ECH2=C(CH3)CH=CH2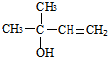 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$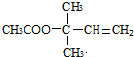 +H2O;
+H2O; .
.