题目内容
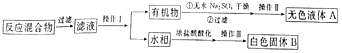
【题目】某酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。利用常用的酸、碱和工业生产中的废铁屑,设计如下工艺流程,从废水中回收金,并生产一定量的铁红和氧化铜。
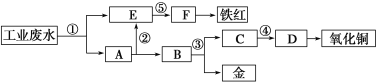
下列说法不正确的是( )
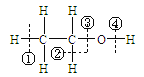
A.标号①②③处发生的反应均为氧化还原反应
B.标号③处加入的相应物质是稀硝酸或稀硫酸
C.标号①处发生的离子反应最多有三个
D.铁红的化学式为Fe2O3,工业上常用作红色颜料
【答案】BC
【解析】
由工艺流程图示知,E为铁元素的离子,而A为铜、金的单质,通过过滤将铁元素与活泼性比它弱的铜、金分离出来,因此①处加入的物质为铁屑,发生的反应为Fe+2H+=Fe2++ H2↑,2Fe3++Fe=3Fe2+,Cu2++Fe=Cu+Fe2+,2Au3++3Fe=2Au + 3Fe2+;②处加入稀硫酸以除去铜、金中过量的铁屑,并将过滤后的硫酸亚铁溶液与含Fe2+的E溶液相混合;③处利用金不溶于硝酸的性质将铜与金分离开;④处将得到的铜离子用氢氧化钠转化为氢氧化铜沉淀,再受热分解为氧化铜;⑤处加入氢氧化钠将亚铁离子转化为氢氧化亚铁沉淀,再利用空气将其转化为氢氧化铁沉淀,最终受热分解为铁红(氧化铁)。
A. 标号①处发生的反应为Fe+2H+=Fe2++ H2↑,2Fe3++Fe=3Fe2+,Cu2++Fe=Cu+Fe2+,2Au3++3Fe=2Au + 3Fe2+,②处发生的反应是Fe+2H+=Fe2++ H2↑;③处发生的反应是铜与稀硝酸生成硝酸铜、一氧化氮、水,均为氧化还原反应,故A正确;
B. 标号③处利用金不溶于硝酸的性质将铜与金分离开,加入的相应物质是稀硝酸,不能是稀硫酸,故B错误;
C. 标号①处发生的离子反应有Fe+2H+=Fe2++ H2↑,2Fe3++Fe=3Fe2+,Cu2++Fe=Cu+Fe2+,2Au3++3Fe=2Au + 3Fe2+,故C错误;
D. Fe2O3是红色粉末,铁红的化学式为Fe2O3,工业上常用作红色颜料,故D正确;
故选BC。

【题目】用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
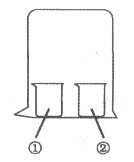
①中的物质 | ②中的物质 | 预测①的现象 | |
A | 淀粉KI溶液 | 浓硝酸 | 无明显变化 |
B | 酚酞溶液 | 浓盐酸 | 无明显变化 |
C | MgCl2溶液 | 浓氨水 | 有白色沉淀 |
D | 湿润红纸条 | 饱和氯水 | 红纸条褪色 |
A. AB. BC. CD. D