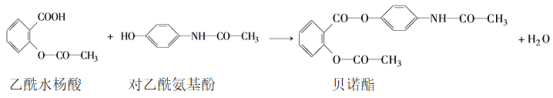
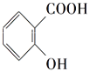
题目内容
【题目】关于乙醇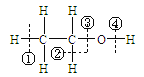 在化学反应中断键位置说法错误的是 ( )
在化学反应中断键位置说法错误的是 ( )
A. 乙醇与浓硫酸在170℃时,在②③位置断裂,以水分子的形式消去,属于消去反应。
B. 乙醇与钠反应,在④位置断裂,对比钠与水反应,乙醇比水更难失去氢离子。
C. 乙醇与浓硫酸在140℃时,在③或④位置断裂,该反应属于取代反应。
D. 乙醇在铜催化下与氧气反应,在②④位置断裂,所以只有与羟基直接相连的碳原子上有氢原子才能发生催化氧化。
【答案】A
【解析】
A. 乙醇和浓硫酸共热到170℃时发生消去反应,断裂碳氧键、与羟基所连的碳的相邻的碳上的碳氢键,即①③断裂,A错误;
B. 乙醇与与金属钠反应生成乙醇钠和氢气,断开的羟基上的氢氧键,即④断裂,对比钠与水反应,乙醇比水更难失去氢离子, 故B正确;
C. 乙醇与浓硫酸在140℃时,在③或④位置断裂,该反应属于取代反应,故C正确;
D. 乙醇在铜催化下与O2反应生成乙醛和水,断开的是羟基上的氢氧键和与羟基所连的碳的氢,即②④断裂,故D正确。
故选A。

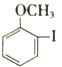
【题目】在一定体积的密闭容器中,进行如下化学反应:其化学平衡常数K与温度t的关系如下:CO2(g)+H2(g) ![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答下列问题:
(1)该反应的化学平衡常数表达式为K =__________________。
(2)该反应为_________反应。(填“吸热”或“放热”)
(3)若反应温度升高,CO2的转化率________(填“增大”“减小”或“不变”);
(4)能判断该反应是否达到化学平衡状态的依据是______。
A.容器中压强不变 B.混合气体中 c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(5)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_____℃。