��Ŀ����
16�����Ӳ�����ͬ�Ķ�����Ԫ��X��Y��Z��W������X��������������K����1��Y��������������K���1��Z�ĵ�����һ�ְ뵼����ϣ�����������̫���ܵ�أ�W��ԭ�Ӱ뾶��ͬ��������С�ģ������ƶ�����ȷ���ǣ�������| A�� | Z����������ˮ��Ӧ���Ƶ���Ӧ�ĺ����� | |
| B�� | X��Y��W������������Ӧˮ����֮�以��ܷ�����Ӧ | |
| C�� | X��Y��W��ԭ�Ӱ뾶���μ�С����Ӧ�����Ӱ뾶�������� | |
| D�� | Z���⻯������ȶ���ǿ��W���⻯�� |
���� ������Ԫ��X��Y��Z��W���Ӳ�����ͬ����X��Y��Z��W����ͬһ���ڣ�Z�ĵ�����һ�ְ뵼����ϣ�����������̫���ܵ�أ���ZΪ��Ԫ�أ�X��������������K����1����X�������1�����ӣ���XΪ��Ԫ�أ�Y��������������K���l����Y�������3�����ӣ���YΪ��Ԫ�أ�W��ԭ�Ӱ뾶��ͬ��������С�ģ���WΪ��Ԫ�أ����Ԫ�������������������жϣ�
��� �⣺������Ԫ��X��Y��Z��W���Ӳ�����ͬ����X��Y��Z��W����ͬһ���ڣ�Z�ĵ�����һ�ְ뵼����ϣ�����������̫���ܵ�أ���ZΪ��Ԫ�أ�X��������������K����1����X�������1�����ӣ���XΪ��Ԫ�أ�Y��������������K���l����Y�������3�����ӣ���YΪ��Ԫ�أ�W��ԭ�Ӱ뾶��ͬ��������С�ģ���WΪ��Ԫ�أ�
A��ZΪ��Ԫ�أ����������Ƕ������裬�������費����ˮ������ˮ��Ӧ����A����
B��X��Y��W������������Ӧˮ����ֱ�Ϊ�������ơ����������������ᣬ���������������������������������ơ������ᷴӦ����������������ᷢ���кͷ�Ӧ����B��ȷ��
C��ͬ����������ң�ԭ�Ӱ뾶��С������ԭ�Ӱ뾶X��Y��W�����Ӳ��Ų���ͬ���˵����Խ�����Ӱ뾶ԽС������Na+��Al3+��������������ͬ�����Ӳ�Խ�����Ӱ뾶Խ������Cl-��Na+���������Ӱ뾶Cl-��Na+��Al3+����C����
D��ZΪ��Ԫ�ء�WΪ��Ԫ�أ�ͬ����������ҷǽ�������ǿ���ǽ�����Cl��Si���ǽ�����Խǿ���⻯��Խ�ȶ�������Z���⻯������ȶ���С��W���⻯���D����
��ѡ��B��
���� ���⿼��ṹ��λ�ù�ϵ��Ԫ�������ɵȣ�Z�ĵ��ʳ���������̫���ܵ�����ƶ�ͻ�ƿڣ��ѶȲ���

| A�� | FeCl3 | B�� | H2O2��Һ | C�� | ŨH2SO4 | D�� | Na2S��Һ |

| A�� | �������Ũ�ȵ�NaOH��Һ��H2A��Һ��Ϻ�����Һ��ˮ�ĵ���̶ȱȴ�ˮС | |
| B�� | H2A��Һ�ڲ�ͬpH�����и����ķֲ���ͬ������ƽ�ⳣ��Ҳ��ͬ | |
| C�� | ��Һ��pH=4.5ʱ���������¹�ϵ��C��Na+����C��HA-����C��A2-����C��H+����C��OH-�� | |
| D�� | ��֪HClO�ĵ���ƽ�ⳣ��Ϊ10-7.5������H2A ����Һ��������NaClO��Һ�У������ķ�ӦΪ��H2A+ClO-�THClO+HA- |
| A�� | �μӼ����Լ��ʺ�ɫ����Һ��Fe2+��NH4+��Cl-��NO3- | |
| B�� | pHΪ11����Һ��S2-��SO32-��S2O32-��Na+ | |
| C�� | ˮ���������c ��OH-��=10-13mol/L����Һ��K+��HCO3-��Br-��Ba2+ | |
| D�� | ��ɫ������Һ��K+��SiO32-��NO3-��Al3+ |
| A�� | ��������ʽ��CH2O | B�� | ��ϩ�Ľṹ��ʽ��CH2CH2 | ||
| C�� | ���Ľṹʽ��C6H6 | D�� | ���廯̼�ĵ���ʽ��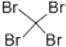 |
| A�� | ����������Һ�����ᷴӦ��OH-+H+=H2O | |
| B�� | �� FeCl2��Һ��ͨ��Cl2��Fe2++Cl2=Fe3++2Cl- | |
| C�� | С�մ���Һ���ռ���Һ��Ӧ��HCO3-+OH-=CO32-+H2O | |
| D�� | ����ͨ����ˮ�У�Cl2+H2O=Cl-+ClO-+2H+ |
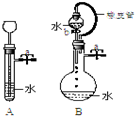 ������ͼ�����ش��������⣺
������ͼ�����ش��������⣺