题目内容
11. 根据如图描述回答下列问题:
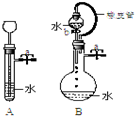
根据如图描述回答下列问题:①关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示.试判断:A装置是否漏气?(填序号)B
A.漏气 B.不漏气 C.不能确定
②关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶.试判断:B装置是否漏气?(填序号)C
A.漏气 B.不漏气 C.不能确定.
分析 检查装置的气密性原理通常是想办法造成装置不同部位有压强差,并产生某种明显现象,如气泡的生成,水柱生成,液面升降.
解答 解:①当通过长颈漏斗向装置A中的试管内加水时,水在长颈漏斗内形成一段水柱,说明试管中密闭气体的压强大于外界大气压,说明装置气密性良好,故答案为:B;
②橡皮管将B装置中两个容器内的气体连通,不管是否漏气,水在重力的作用下总能往烧瓶中流入,因此无法确定装置B是否漏气,故答案为:C.
点评 本题考查气体气密性的检查,为高频考点,侧重于学生的分析能力和实验能力的考查,答题时注意:一是怎样增大体系内气体的压强;二是能否正确地描述实验现象.通过对问题的回答,难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
12.甲、乙、丙、丁4种溶液中各含一种Xn-离子(Xn-可以代表Cl-、Br-、I-、S2-中任意一种)先向甲中加人淀粉溶液和氯水,溶液变橙色.再加入丙溶液,颜色没有明显变化,最后向溶液中加入丁溶液,溶液褪色且浑浊.则甲、乙、丙、丁中依次含有的离子为( )
| A. | Br-,I-,Cl-,S2- | B. | Br-,Cl-,I-,S2- | C. | Br-,Cl-,S2-,I- | D. | Cl-,I-,S2--,Br- |
19.下列有关比较中,大小顺序排列错误的是( )
| A. | 热稳定性:PH3>H2S>HBr>NH3 | |
| B. | 物质的熔点:石英>食盐>冰>汞 | |
| C. | 结合质子的能力:CO32->CH3COO->SO42- | |
| D. | 分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
6.实验中需用2.0mol/L的Na2CO3溶液950ml,配制时应选用的容量瓶的规格和称取的质量分别为( )
| A. | 950ml;201.4g | B. | 1000ml; 212g | C. | 100ml; 21.2g | D. | 500ml; 100.7g |
16.电子层数相同的短周期元素X、Y、Z、W,其中X的最外层电子数比K层少1,Y的最外层电子数比K层多1,Z的单质是一种半导体材料,常用于制造太阳能电池,W的原子半径是同周期中最小的.下列推断中正确的是( )
| A. | Z的氧化物与水反应可制得相应的含氧酸 | |
| B. | X、Y、W的最高价氧化物对应水化物之间互相都能发生反应 | |
| C. | X、Y、W的原子半径依次减小,对应的离子半径依次增大 | |
| D. | Z的氢化物的热稳定性强于W的氢化物 |
20.下列溶液中导电能力最强的是( )
| A. | 150mL0.2mol/L氢氧化钠溶液 | B. | 100mL0.3mol/L醋酸溶液 | ||
| C. | 200mL0.2mol/L硫酸溶液 | D. | 150mL0.2mol/L盐酸溶液 |
1.向含有1mol明矾的溶液中逐滴加入Ba(OH)2溶液,充分反应,下列说法不正确的是( )
| A. | 当Al3+恰好完全沉淀时,消耗Ba(OH)2 1.5 mol | |
| B. | 当SO42-恰好完全沉淀时,Al3+全部转化为Al(OH)3 | |
| C. | 当向溶液中加入1.5 mol Ba(OH)2时,反应可用下列离子方程式表示:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| D. | 随着加入的Ba(OH)2的物质的量不断增大,沉淀的物质的量不断增大 |
 工业上常用铁质容器盛装冷浓硫酸.为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
工业上常用铁质容器盛装冷浓硫酸.为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动: .
.