题目内容
7.D是一种单质,化合物A、B、C都只含有两种元素,且A、B、D均含X元素.已知一定条件下可发生反应:A+B═C+D,由此可知X元素( )| A. | 一定是金属元素 | |
| B. | 一定是非金属元素 | |
| C. | 可能是金属元素,也可能是非金属元素 | |
| D. | 以上均不正确 |
分析 根据题意:(1)A、B、C都是化合物;(2)A、B均含X元素;(3)反应生成单质X,可以推知该反应为“归中型”氧化还原反应.即化合物A、B中X元素的化合价“一高一低”(一个高于0价、一个低于0价),两者共同作用生成X单质(化合价为0).由于金属元素在化合物中只呈现正价态,不可能有负价态,因此可以肯定X不是金属元素;只有非金属元素在化合物中才既可呈正价态,又可呈负价态,并在一定条件下可以发生归中反应.
解答 解:根据题意:(1)A、B、C都是化合物;(2)A、B均含X元素;(3)反应生成单质X,可以推知该反应为“归中型”氧化还原反应.即化合物A、B中X元素的化合价“一高一低”(一个高于0价、一个低于0价),两者共同作用生成X单质(化合价为0).由于金属元素在化合物中只呈现正价态,不可能有负价态,因此可以肯定X不是金属元素;只有非金属元素在化合物中才既可呈正价态,又可呈负价态,并在一定条件下可以发生归中反应.例如:2H2S+SO2=3S↓+2H2O,4NH3+6NO=5N2+6H2O,所以X应该是非金属,即该题的答案为B.
故选B.
点评 本题考查无机物推断,属于开放性题目,需要学生熟练掌握氧化还原反应知识等,注意把握“归中型”氧化还原反应及元素性质,题目难度中等.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
17.短周期元素R、W、X、Y、Z的原子序数依次增大,R原子的最外层电子数是其内层电子数的2倍,X元素的焰色反应呈黄色,W元素和Z元素同主族,且Z元素的核电荷数是W的2倍,Y是地壳中除氧外含量最多的非金属元素.下列说法不正确的是( )
| A. | W与X形成的两种化合物中阴、阳离子的个数比均为1:2 | |
| B. | Y、R、Z最高价氧化物对应水化物的酸性强弱顺序:Z>R>Y | |
| C. | W的氢化物熔沸点比Z的氢化物熔沸点低 | |
| D. | Y与R形成的化合物YR的熔点高、硬度大 |
18.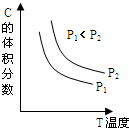 已知某可逆反应aA(g)+bB(g)?cC(g)+dD(l);△H=-E KJ•mol-1.反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图.下列叙述正确的是( )
已知某可逆反应aA(g)+bB(g)?cC(g)+dD(l);△H=-E KJ•mol-1.反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图.下列叙述正确的是( )
 已知某可逆反应aA(g)+bB(g)?cC(g)+dD(l);△H=-E KJ•mol-1.反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图.下列叙述正确的是( )
已知某可逆反应aA(g)+bB(g)?cC(g)+dD(l);△H=-E KJ•mol-1.反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图.下列叙述正确的是( )| A. | 正反应为吸热反应 | |
| B. | 100摄氏度时,当生成cmolC,放出E KJ热量 | |
| C. | a+b<c+d | |
| D. | 降低压强,正、逆反应速率都减小 |
16.现有下列几组粒子:①N2、CO;②NH4+、OH-;③O22-、CN-;④PO43-、ClO4-.对上述四组粒子归类正确的是( )
| A. | 质子数相等、电子数和原子数不相等:① | |
| B. | 质子数和电子数相等、原子数不相等:② | |
| C. | 电子数相等、质子数和原子数不相等:③ | |
| D. | 原子数和电子数相等、质子数不相等:④ |
 ;
;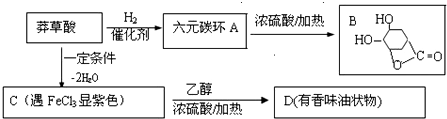
 .
.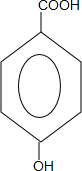 +CH3CH2OH$→_{△}^{浓硫酸}$H20+
+CH3CH2OH$→_{△}^{浓硫酸}$H20+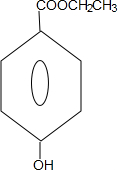 .
.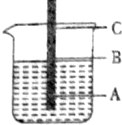 一根铁丝插入煮沸过的蒸馏水中,铁丝上有三点,问:
一根铁丝插入煮沸过的蒸馏水中,铁丝上有三点,问: