题目内容
15.A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.请回答下列问题:
(l)B的原子结构示意图
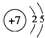 ;
;(2)C、D、E三种原子对应的离子半径由大到小的顺序是S2->O2->Na+ (填具体离子符号);由A、B、C三种元素按 4:2:3组成的化合物所含的化学键类型属于离子键、共价键.
(3)用某种废弃的金属易拉罐与 A、C、D组成的化合物溶液反应,该反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(4)C和E两元素相比较,非金属性较强的是氧(填“元素名称”),可以验证该结论的是CD (填“序号”).
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素的单质在常温下的状态
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(5)A、C两元素的单质与熔融K2CO3组成的燃料电池,其负极反应式H2+CO32--2e-=CO2↑+H2O;用该电池电解lLlmol/LNaCl溶液,当消耗标准状况下1.l2LA2时,NaCl溶液的pH=13 (假设电解过程中溶液的体积不变)
分析 A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和C可形成两种常见的液态化合物,则A为H元素、C为O元素,二者形成的液态化合物为H2O、H2O2,A和D最外层电子数相同,二者同主族,结合原子序数可知,D为Na;B、C和E在周期表中相邻,且C、E同主族,B、C的最外层电子数之和等于D的原子核外电子数,则B、C最外层电子数分别为5、6,可推知B为N元素、C为O元素、E为S元素,据此解答.
解答 解:A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和C可形成两种常见的液态化合物,则A为H元素、C为O元素,二者形成的液态化合物为H2O、H2O2,A和D最外层电子数相同,二者同主族,结合原子序数可知,D为Na;B、C和E在周期表中相邻,且C、E同主族,B、C的最外层电子数之和等于D的原子核外电子数,则B、C最外层电子数分别为5、6,可推知B为N元素、C为O元素、E为S元素.
(l)B为N元素,原子结构示意图为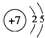 ,故答案为:
,故答案为: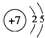 ;
;
(2)C、D、E三种原子对应的离子分别为O2-、Na+、S2-,电子层结构相同的离子,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径:S2->O2->Na+;
由H、N、O三种元素按 4:2:3组成的化合物为NH4NO3,所含的化学键有:离子键、共价键,
故答案为:S2->O2->Na+;离子键、共价键;
(3)金属易拉罐含有金属Al,A、C、D组成的化合物为NaOH,二者该反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)氧与硫同主族,从上到下非金属性在减弱,则非金属性O>S,
A.沸点属于物理性质,不能比较元素的非金属性强弱,故A错误;
B.单质的状态属于物理性质,不能比较元素的非金属性强弱,故B错误;
C.气态氢化物的稳定性,元素的非金属性越强,可以利用氢化物稳定性比较,故C正确;
D.元素的单质与氢气化合的越容易,单质越活泼,元素的非金属性越强,故D正确;
故答案为:氧;CD;
(5)氢气、氧气与熔融K2CO3,组成的燃料电池,氢气在负极放电,在熔融碳酸钾条件下生成二氧化碳与水,电解反应式为:H2+CO32--2e-=CO2↑+H2O;
用该电池电解1L 1mol/LNaCl溶液,当消耗标准状况下1.12LH2时,氢气的物质的量=$\frac{1.12L}{22.4L/mol}$=0.05mol,生成的NaOH物质的量=0.05mol×2=0.1mol,故n(OH-)=0.1mol/L,则c(H+)=$\frac{1{0}^{-14}}{0.1}$=10-13,故l溶液的pH=-lg10-13=13,
故答案为:H2+CO32--2e-=CO2↑+H2O;13.
点评 本题考查结构性质位置关系综合应用,推断元素是解题关键,涉及原子结构示意图、微粒半径比较、化学键、原电池与电解、化学计算、非金属性比较等,难度中等,是对知识综合运用与学生能力考查,难度中等.

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案| A. | HCl、CuCl2、Ba(OH)2 | B. | NaOH、CuSO4、H2SO4 | ||
| C. | NaOH、H2SO4、Ba(OH)2 | D. | NaBr、H2SO4、Ba(OH)2 |
| A. | 地震灾区用漂白粉消毒,是利用漂白粉溶液的碱性 | |
| B. | 铝热反应是工业炼铁常用的方法 | |
| C. | 生铁在潮湿的空气中易生锈,其负极反应式为2H2O+02+4e-═4OH- | |
| D. | 实验室储存的钠着火时,可以用砂子盖灭 |
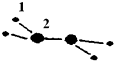 (1)M由两种短周期元素组成,每个M分子含有18个电子,其分子球棍模型如图所示.测得M的摩尔质量为32g/mol.画出编号为2的原子结构示意图:
(1)M由两种短周期元素组成,每个M分子含有18个电子,其分子球棍模型如图所示.测得M的摩尔质量为32g/mol.画出编号为2的原子结构示意图: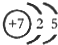 .
.(2)已知1.0mol•L-1NaHSO3溶液的pH为3.5,加入氯水,振荡后溶液pH迅速降低.溶液pH降低的原因是HSO3-+Cl2+H2O=3H++SO42-+2Cl-(用离子方程式表示).
(3)在常温常压和光照条件下,N2在催化剂(TiO2)表面与H2O反应,生成1molNH3和O2时的能量变化值为382.5kJ,达到平衡后此反应NH3生成量与温度的实验数据如下表.则该反应的热化学方程式为$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2O(l)?NH3(g)+$\frac{3}{4}$O2(g)△H=+382.5kJ/mol(或2N2(g)+6H2O(l)?4NH3(g)+3O2(g)△H=+1530.0kJ/mol).
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-1mol) | 4.3 | 5.9 | 6.0 |
2NH4+(aq)+Mg(OH)2(s)?Mg2+(aq)+2NH3•H2O(aq)
写出上述反应的平衡常数表达式K=$\frac{c(M{g}^{2+})•{c}^{2}(N{H}_{3}•{H}_{2}O)}{{c}^{2}(N{{H}_{4}}^{+})}$
某研究性学习小组为探究Mg2+与NH3•H2O反应形成沉淀的情况,设计如下两组实验
| 实验① | 等体积1mol/L氨水和0.1mol/L MgCl2溶液混合 | 生成白色沉淀 |
| 实验② | 等体积0.1mol/L氨水和1mol/L MgCl2溶液混合 | 无现象 |
(5)在室温下,化学反应I-(aq)+ClO-(aq)=IO-(aq)+Cl-(aq)的反应物初始浓度、溶液中的氢氧根离子初始浓度及初始速率间的关系如下表所示:
| 实验编号 | I-的初始浓度 (mol•L-1) | ClO-的初始浓度 (mol•L-1) | OH-的初始浓度 (mol•L-1) | 初始速率v (mol•L-1•s-1) |
| 1 | 2×10-3 | 1.5×10-3 | 1.00 | 1.8×10-4 |
| 2 | a | 1.5×10-3 | 1.00 | 3.6×10-4 |
| 3 | 2×10-3 | 3×10-3 | 2.00 | 1.8×10-4 |
| 4 | 4×10-3 | 3×10-3 | 1.00 | 7.2×10-4 |
①设计实验2和实验4的目的是探究ClO-对反应速率的影响;
②若实验编号4的其它浓度不变,仅将溶液的酸碱值变更为pH=13,反应的初始速率v=7.2×10-4.
| A. | 一定是金属元素 | |
| B. | 一定是非金属元素 | |
| C. | 可能是金属元素,也可能是非金属元素 | |
| D. | 以上均不正确 |
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化
①已知部分化学键的键能如下(键能指气态原子形成1mol化学键释放的最小能量)
| 化学键 | N=O | C≡O | C=O | N≡N |
| 键能(kj/mol) | 632 | 1072 | 750 | 946 |
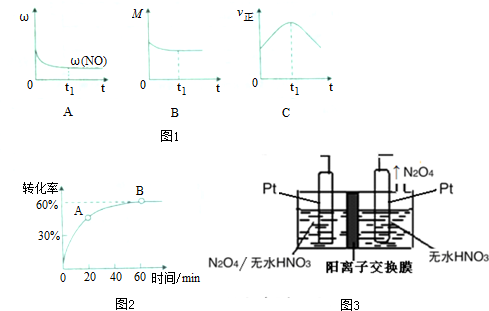
②若上述反应在绝热、恒荣的密闭体系中进行,并在t1时到达平衡状态,则下列示意图不符合题意的是C(填选项序号)(图中1ω、M、?、z分别表示质量分数、混合气体平均相对分子质量、正反应速率)
(2)尾气中的SO2可先催化氧化生成SO2,再合成硫酸,已知:
2SO${\;}_{{\;}_{2}}$(g)+O2(g)$?_{高温}^{催化剂}$2SO2(g)△H=-196.0kj/mol
①在一定温度的密闭容器中,SO2的转化率时间的变化关系如图2所示,则A点的正反应速率v正(SO2)<B点的正反应速率v正(SO2)(填“大于”、“小于”或“等于”)
②在某温度时,向10L的密闭容器中加入4.0mol SO2和10.0mol O2,反应达到平衡,改变下列条件,再次达到平衡时,能使O2的新平面浓度和原来平衡浓度相同的是BC(填选项序号)
A.在其他条件不变时,减少容器的容积
B.保持温度和容器内压强不变,再充入2.0mol SO2和5.0mol O2
C.保持温度和容器体积不变,再充入SO2和SO3,使之浓度扩大为原来的两倍
(3)用NH3催化还原NO2也可以消除氮氧化物的污染,反应原理为:
NO(g)+NO2(g)+2NH3(g)?2N2(g)+3H2O(g)
对于气体反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cb)也可以表示平衡常数(记作Kp),则上述反应的K的表达式为$\frac{{p}^{3}({H}_{2}O){p}^{2}({N}_{2})}{p(NO)p(N{O}_{2}){p}^{2}(N{H}_{3})}$
(4)以N2O4为原料采用电解法可制备新型绿色硝化剂N2O3,实验装置如图3所示,电解池中生成N2O3的电极反应式为N2O4+2HNO3-e-=2N2O3+O2↑+2H+
(5)尾气中氢氧化物(NO和NO2)可用尿素[CO(NH2)3]溶液除去,反应生成对大气无污染的气体,1mol尿素能吸收工业尾气中氢氧化物(假设NO、NO2体积比为1:1)的质量为76g.
 元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素.Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,其空间构型为v形,W的基态原子3d轨道有8种运动状态不同的电子.请回答下列问题:
元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素.Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,其空间构型为v形,W的基态原子3d轨道有8种运动状态不同的电子.请回答下列问题: