题目内容
15.下列关于仪器使用的说法正确的是( )| A. | 在量取液体后,量筒中残留的液体要用蒸馏水洗涤并转入相应容器 | |
| B. | 熔融纯碱、烧碱时,不能选用石英坩埚,应该选用铁坩埚 | |
| C. | 蒸发结晶实验中,蒸发皿应放在石棉网上加热 | |
| D. | 在测量或监测温度时,温度计水银球碰到容器内壁不影响测量结果 |
分析 A.量筒不能洗涤,否则会导致量取的液体的量偏大;
B.石英坩埚的主要成分为二氧化硅,二氧化硅能够与碱溶液反应;
C.蒸发皿是可以直接加热的仪器;
D.温度计的水银球不能接触容器内壁,否则会影响测定结果.
解答 解:A.在量取液体后,量筒中残留的液体不能用蒸馏水洗涤并转入相应容器,否则会导致量取的液体体积偏大,故A错误;
B.熔融纯碱、烧碱时,由于碱溶液能够与二氧化硅反应,所以不能选用石英坩埚,可以选用铁坩埚,故B正确;
C.蒸发结晶实验中,蒸发皿可以直接加热,不需要放在石棉网上加热,故C错误;
D.测量或监测温度时,温度计水银球不能碰到容器内壁,否则读数不准确,会影响测量结果,故D错误;
故选B.
点评 本题考查了常见仪器的使用方法,题目难度不大,注意掌握常见仪器的构造及正确的使用方法,明确常见的可以直接加热仪器、不能加热仪器及需要垫上石棉网加热仪器的名称.

练习册系列答案
相关题目
6.下列离子方程式书写正确的是( )
| A. | 澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O | |
| B. | 氢氧化钡溶液与稀硫酸的反应:OH-+H+=H2O | |
| C. | 用FeCl3溶液腐蚀印刷电路板上铜箔:2Fe3++Cu=2Fe+Cu2+ | |
| D. | 碳酸钙溶于稀盐酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
3.甲、乙两种非金属:①甲比乙容易与氢气化合;②甲原子能与乙的阴离子发生置换反应;③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;④与某金属反应时,甲原子得电子数目比乙的多;⑤甲的单质熔、沸点比乙的低.能说明甲比乙的非金属性强的是( )
| A. | 只有④ | B. | 只有⑤ | C. | ①②③ | D. | ①②③④⑤ |
10.甲、乙是元素周期表中同一周期的两种元素,甲位于ⅡA族,其原子序数为x,乙位于ⅢA族,则乙的原子序数可能是( )
①x+1 ②x+11 ③x+25 ④x+26 ⑤x+10.
①x+1 ②x+11 ③x+25 ④x+26 ⑤x+10.
| A. | ① | B. | ②③ | C. | ①②③ | D. | 全部 |
20.同周期的X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是:HZO4>H2YO4>H3XO4,下列判断正确的是( )
①阴离子的还原性按X、Y、Z顺序减弱
②单质的氧化性按X、Y、Z顺序增强
③元素的原子半径按X、Y、Z顺序减小
④气态氢化物的稳定性按X、Y、Z顺序减弱.
①阴离子的还原性按X、Y、Z顺序减弱
②单质的氧化性按X、Y、Z顺序增强
③元素的原子半径按X、Y、Z顺序减小
④气态氢化物的稳定性按X、Y、Z顺序减弱.
| A. | ①② | B. | ②③ | C. | ①②③ | D. | ①②③④ |
7.下列实验中不能出现沉淀现象的是( )
| A. | NO2 和SO2气体同时通入BaCl2溶液中 | |
| B. | SO2气体通入BaCl2溶液中 | |
| C. | SO2气体通入Ba(NO3)2溶液中 | |
| D. | SO2气体和过量NH3 同时通入BaCl2溶液中 |
5.将一定质量的Mg、Cu组成的混合物投入适量稀硝酸中,固体恰好完全溶解时收集到标准状况下0.896LNO气体,向反应后溶液中加入2mol/L NaOH溶液70mL时金属离子恰好沉淀完全.则整个过程消耗的硝酸的物质的量为( )
| A. | 0.18mol | B. | 0.16mol | C. | 0.14mol | D. | 0.12mol |
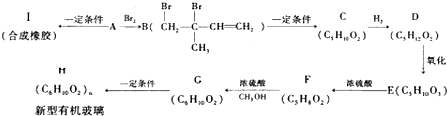
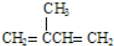 (不考虑立体异构),由G生成H的反应类型是加聚反应;
(不考虑立体异构),由G生成H的反应类型是加聚反应;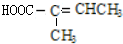 +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$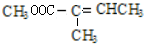 +H2O.与F具有相同官能团且比F少一个碳原子的有机物的同分异构体有3种(不考虑立体异构);
+H2O.与F具有相同官能团且比F少一个碳原子的有机物的同分异构体有3种(不考虑立体异构);