题目内容
3.甲、乙两种非金属:①甲比乙容易与氢气化合;②甲原子能与乙的阴离子发生置换反应;③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;④与某金属反应时,甲原子得电子数目比乙的多;⑤甲的单质熔、沸点比乙的低.能说明甲比乙的非金属性强的是( )| A. | 只有④ | B. | 只有⑤ | C. | ①②③ | D. | ①②③④⑤ |
分析 根据与氢化合的难易程度、单质之间的置换反应、最高价氧化物对应的水化物酸性、气态氢化物的稳定性等来比较非金属性的强弱,以此来解答.
解答 解:①甲比乙容易与H2化合,则甲的非金属性强,故正确;
②甲单质能与乙阴离子发生置换反应,即甲置换出乙,所以甲的非金属性强,故正确;
③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强,则非金属性甲大于乙,故正确;
④与某金属反应时,甲原子得电子数目比乙的多,不能比较非金属性的强弱,故错误;
⑤甲的单质熔、沸点比乙的低,不能利用物理性质比较非金属性的强弱,故错误;
故选C.
点评 本题考查非金属性的比较,注意归纳常见的非金属性比较的方法是解答此类习题的关键,侧重学生归纳整合知识的能力考查,注重学生的基础,题目难度不大.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
14.向100mLFeCl3 溶液中通入标准状况下的H2S气体3.36L,设 H2S全部被吸收后,再加入过量的铁粉,待反应停止后,测得溶液中含有0.6mol金属阳离子,则原FeCl3溶液的物质的量浓度为( )
| A. | 5.0 m o l/L | B. | 4.0 m o l/L | C. | 4.5 m o l/L | D. | 3.0 m o l/L |
11.下列有关元素周期表的说法正确的是( )
| A. | 对于元素周期表和元素周期律的发现有突出贡献的科学家是阿伏加德罗 | |
| B. | 元素周期表根据相对原子质量从小到大的顺序排列 | |
| C. | 现常见的元素周期表有七个横行,分为七个周期,有18个纵行,分为16个族 | |
| D. | 每一周期都是从金属元素开始,非金属元素结束 |
18.已知乙烯能被酸性高锰酸钾溶液氧化成CO2,既可用来鉴别乙烷和乙烯,又可用来除去乙烷中混有的乙烯的方法是( )
| A. | 通入足量溴水中 | B. | 分别在空气中燃烧 | ||
| C. | 通入酸性高锰酸钾溶液中 | D. | 在一定条件下通入氢气 |
15.下列关于仪器使用的说法正确的是( )
| A. | 在量取液体后,量筒中残留的液体要用蒸馏水洗涤并转入相应容器 | |
| B. | 熔融纯碱、烧碱时,不能选用石英坩埚,应该选用铁坩埚 | |
| C. | 蒸发结晶实验中,蒸发皿应放在石棉网上加热 | |
| D. | 在测量或监测温度时,温度计水银球碰到容器内壁不影响测量结果 |
13.下列说法中错误的是( )
| A. | 所有的非金属元素都分布在P区 | |
| B. | 除氦外的稀有气体原子的最外层电子数都是8 | |
| C. | 原子的核外电子层数等于该元素所在的周期数 | |
| D. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 |
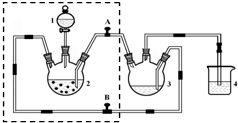 醋酸亚铬水合物([Cr(CH3COO)2)]2•2H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,微溶于醇,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下:
醋酸亚铬水合物([Cr(CH3COO)2)]2•2H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,微溶于醇,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下:
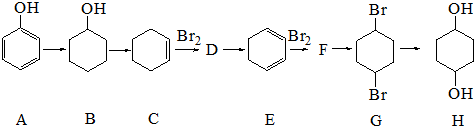
 +2NaOH$\stackrel{醇△}{→}$
+2NaOH$\stackrel{醇△}{→}$ +2NaBr+2H2O.
+2NaBr+2H2O.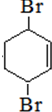 .
. +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2 +2H2O.
+2H2O.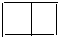 .
.