题目内容
13.下列物质互为同分异构体的是( )| A. | 1-丁烯和1,3-丁二烯 | B. | 己烷和环己烷 | ||
| C. | 尿素和氰酸铵(NH4CNO) | D. | 1,4-二甲苯和1,3,5-三甲苯 |
分析 同分异构体是指分子式相同,但结构不同的化合物,以此来解答.
解答 解:A、两者分子式不同,且1,3-丁二烯中含有2个碳碳双键,故与1-丁烯不是同分异构体,故A错误;
B、己烷与环己烷的分子式不同,不是同分异构体,故B错误;
C、氰酸铵NH4CNO与尿素CO(NH2)2是分子式相同,结构不同的两种化合物,互称为同分异构体,故C正确;
D、1,4-二甲苯和1,3,5-三甲苯分子式分别为:C8H10和C9H12,不是同分异构体,故D错误.
故选C.
点评 本题考查了有机化合物的同分异构体的判断和理解,掌握概念实质是解题关键,题目较简单.

练习册系列答案
相关题目
3.50mL18mol/L的H2SO4中加入足量的铜片并加热,被还原的H2SO4的物质的量为( )
| A. | <0.45mol | B. | 0.45mol | ||
| C. | 0.45-0.90mol之间 | D. | >0.90mol |
4.甲烷燃烧和氢气燃烧的热化学方程式如下:
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1
2H2(g)+O2(g)═2H2O(g)△H2
2H2(g)+O2(g)=2H2O(l)△H3
常温下取体积为4:1的甲烷和氢气混合气体11.2L(标况),完全燃烧后恢复常温,放出热量为( )
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1
2H2(g)+O2(g)═2H2O(g)△H2
2H2(g)+O2(g)=2H2O(l)△H3
常温下取体积为4:1的甲烷和氢气混合气体11.2L(标况),完全燃烧后恢复常温,放出热量为( )
| A. | 0.4△H1+0.05△H3 | B. | 0.4△H1+0.05△H2 | C. | 0.4△H1+0.1△H3 | D. | 0.4△H1+0.2△H3 |
8.已知:t℃时,2H(g)+Y(g)?2I(g)△H=-196.6kJ•mol-1,t℃时,在一压强恒定的密闭容器中,加入4mol H和2mol Y反应,达到平衡后,Y剩余0.2mol.若在上面的平衡体系中,再加入1mol气态的I物质,t℃时达到新的平衡,此时H物质的物质的量n(H)为( )
| A. | 0.8 mol | B. | 0.6 mol | C. | 0.5 mol | D. | 0.2 mol |
18.A、B、C三种元素的核电荷数依次为a、b、c,它们的离子An+、Bn-、Cm-具有相同的电子层结构,且n>m,则下列关系正确的是( )
| A. | a>b>c | B. | a>c>b | C. | a=b+m+n | D. | a=c+n+m |
2.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
| A. | CO2的电子式 | B. | Cl-的结构示意图: | ||
| C. | 乙烯的结构简式C2H4 | D. | Z质量数为37的氯原子${\;}_{37}^{17}$Cl |
3. 现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题
现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题
(1)B基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形.
(2)C和与其左右相邻元素原子的第一电离能由大到小的顺序是Mg>Al>Na.
(3)①DE3中心原子的杂化方式为sp3杂化,该分子中的键角比离子DE4+中的键角小的原因是孤电子对与成键电子对的排斥作用力大于成键电子对之间的排斥作用力
②将E的单质通入到黄血盐{K4[Fe(CN)6]}溶液中,可得到赤血盐{K3[Fe(CN)6]}.该反应的离子方程式为2[Fe(CN)6]4-+Cl2=2[Fe(CN)6]3-+2Cl-
③已知含E的一种化合物与过氧化氢发生如下反应(已配平):H2O2+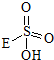 →
→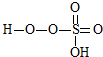 +HE,请写出横线上物质的结构式.
+HE,请写出横线上物质的结构式.
(4)F位于d区,价电子排布式为3d54s1.
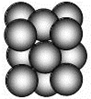
(5)G单质晶体中原子的堆积方式为面心立方最密堆积(如图),则晶胞中每个原子的配位数为12.假设晶胞边长为a,原子半径为r,列式表示该晶胞的空间利用率为$\frac{\sqrt{2}}{6}π$.
 现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题
现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F 是前四周期原子电子轨道表示式中单电子数最多的元素 |
| G在周期表的第十一列 |
(2)C和与其左右相邻元素原子的第一电离能由大到小的顺序是Mg>Al>Na.
(3)①DE3中心原子的杂化方式为sp3杂化,该分子中的键角比离子DE4+中的键角小的原因是孤电子对与成键电子对的排斥作用力大于成键电子对之间的排斥作用力
②将E的单质通入到黄血盐{K4[Fe(CN)6]}溶液中,可得到赤血盐{K3[Fe(CN)6]}.该反应的离子方程式为2[Fe(CN)6]4-+Cl2=2[Fe(CN)6]3-+2Cl-
③已知含E的一种化合物与过氧化氢发生如下反应(已配平):H2O2+
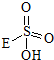 →
→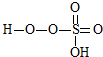 +HE,请写出横线上物质的结构式.
+HE,请写出横线上物质的结构式.(4)F位于d区,价电子排布式为3d54s1.
(5)G单质晶体中原子的堆积方式为面心立方最密堆积(如图),则晶胞中每个原子的配位数为12.假设晶胞边长为a,原子半径为r,列式表示该晶胞的空间利用率为$\frac{\sqrt{2}}{6}π$.
 已知化合物A、B、C、D、E、F、G和单质甲、乙所含元素均为短周期元素,A的浓溶液与甲能发生如图所示的反应.甲是常见的黑色固体单质,乙是常见的气体单质,是空气的主要成分之一,B是无色气体,是主要的大气污染物之一,C常温下为无色液体,E是一种淡黄色的固体.请回答下列问题.
已知化合物A、B、C、D、E、F、G和单质甲、乙所含元素均为短周期元素,A的浓溶液与甲能发生如图所示的反应.甲是常见的黑色固体单质,乙是常见的气体单质,是空气的主要成分之一,B是无色气体,是主要的大气污染物之一,C常温下为无色液体,E是一种淡黄色的固体.请回答下列问题.

 .
.