题目内容
18.A、B、C三种元素的核电荷数依次为a、b、c,它们的离子An+、Bn-、Cm-具有相同的电子层结构,且n>m,则下列关系正确的是( )| A. | a>b>c | B. | a>c>b | C. | a=b+m+n | D. | a=c+n+m |
分析 A、B、C三种元素的核电荷数依次为a、b、c,它们的离子An+、Bn-、Cm-具有相同的电子层结构,且n>m,根据阳离子的电子数=质子数-电荷数,阴离子的电子数=质子数+电荷数,据此分析.
解答 解:A.A、B.三种元素的核电荷数依次为a、b、c,它们的离子An+、Bn-、Cm-具有相同的电子层结构,且n>m,则电子数相同,所以a-n=b+n=c+m,则原子序数a>c>b,故A错误;
B.根据A知,原子序数a>c>b,故B正确;
C.由分析可知a-n=b+n=c+m,则a=b+2n,故C错误;
D.由分析可知a-n=b+n=c+m,则a=c+n+m,故D正确.
故选BD.
点评 本题考查了原子的结构,题目难度不大,注意把握阴阳离子中质子数与电子数的关系.

练习册系列答案
相关题目
8.有Wn+、Xm+、Ym-、Zn-(m>n)四种主族元素离子,且W、X、Y、Z四种原子的M电子层中的电子数均为奇数.下列说法中正确的是( )
| A. | Wn+、Xm+、Ym-、Zn-的离子半径依次增大 | |
| B. | Y、Z的气态氢化物的热稳定性:HmY>HnZ | |
| C. | W、X、Y、Z的最高价氧化物对应的水化物都是强电解质 | |
| D. | W、X、Y、Z的最高价氧化物对应的水化物的碱性依次减弱,酸性依次增强 |
9.第三周期元素中非金属性最强的是( )
| A. | Al | B. | Cl | C. | Mg | D. | Si |
6.下列实验事实不能用平衡移动原理解释的是( )
| A. |  将NO2球浸泡在冷水中和热水中 | |
| B. | 排饱和食盐水收集氯气 | |
| C. | 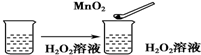 | |
| D. | N2+3H2$?_{催化剂}^{高温、高压}$2NH3△H<0工业合成氨,通常选择高压的条件 |
13.下列物质互为同分异构体的是( )
| A. | 1-丁烯和1,3-丁二烯 | B. | 己烷和环己烷 | ||
| C. | 尿素和氰酸铵(NH4CNO) | D. | 1,4-二甲苯和1,3,5-三甲苯 |
3.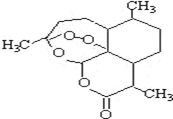 被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )
被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )
 被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )
被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )| A. | 分子式为:C16H22O5 | |
| B. | 该化合物在一定条件下不能与NaOH溶液反应 | |
| C. | 该化合物中含有过氧键,一定条件下有氧化性 | |
| D. | 青蒿素易溶于水 |
10.原电池的总反应为:Zn+H2SO4=ZnSO4+H2↑,负极上发生反应的物质是( )
| A. | H2SO4 | B. | Zn | C. | ZnSO4 | D. | H2 |
7.下列对于Na、Mg、Al的有关性质的叙述中,正确的是( )
| A. | 离子的氧化性:Na+>Mg2+>Al3+ | B. | 原子半径:Al>Mg>Na | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 单质的还原性:Na<Mg<Al |