题目内容
【题目】下列事实,不能用勒夏特列原理解释的是( )
A.溴水中有平衡:Br2+H2O![]() HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅
HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅
B.对CO(g) + NO2 (g)![]() CO2(g)+ NO(g) 平衡体系增大压强可使颜色变深
CO2(g)+ NO(g) 平衡体系增大压强可使颜色变深
C.高压比常压有利于合成SO3的反应
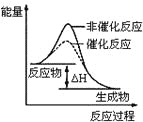
D.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施
【答案】B
【解析】
A.溴水中有平衡:Br2+ H2O![]() HBr+ HBrO 加入 AgNO3溶液后,消耗溴离子平衡右移溶液颜色变浅,符合勒夏特列原理,故A不选;
HBr+ HBrO 加入 AgNO3溶液后,消耗溴离子平衡右移溶液颜色变浅,符合勒夏特列原理,故A不选;
B.CO(g) + NO2 (g)![]() CO2(g)+ NO(g) 平衡体系增大压强平衡不移动,颜色变深是因为体积变小,不符合勒夏特列原理,故B可选;
CO2(g)+ NO(g) 平衡体系增大压强平衡不移动,颜色变深是因为体积变小,不符合勒夏特列原理,故B可选;
C.2SO2+O2![]() 2SO3增加压强向正反应方向移动,符合勒夏特列原理,故C不选;
2SO3增加压强向正反应方向移动,符合勒夏特列原理,故C不选;
D.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施,因为正反应方向为放热反应,故D不选;
故答案选B。

【题目】酸性![]() 溶液与
溶液与![]() 溶液反应的离子方程式为:
溶液反应的离子方程式为:![]() ,某同学设计如下表所示方案探究温度、浓度改变对该反应速率的影响情况。
,某同学设计如下表所示方案探究温度、浓度改变对该反应速率的影响情况。
实验序号 | 实验温度 | 参加反应的物质 | 溶液颜色褪至无色所需时间 | ||||
|
|
| |||||
|
|
|
|
| |||
A | 298 | 2 |
| 4 | a | 0 |
|
B |
| 2 |
| 3 | a |
| 10 |
C | 318 | 2 |
|
| a | 1 |
|
(1)实验中a的最小值为____________,探究温度变化对反应速率影响情况的两组实验是________。
(2)![]() ____________,
____________,![]() ____________,利用实验B中数据计算,用
____________,利用实验B中数据计算,用![]() 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为![]() ________。
________。
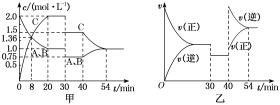
(3)他们发现,A组实验中收集的![]() 体积如图a所示;若使A组反应在绝热容器中进行,该反应的反应速率随着时间的变化如图b所示。
体积如图a所示;若使A组反应在绝热容器中进行,该反应的反应速率随着时间的变化如图b所示。
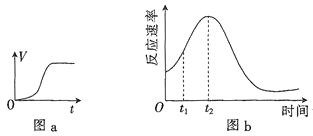
![]() 时间内速率变快的主要原因可能是:一是产物中
时间内速率变快的主要原因可能是:一是产物中![]() 是反应的催化剂;二是______________________________。
是反应的催化剂;二是______________________________。
![]() 由图b信息知,催化剂的催化效果与其用量________
由图b信息知,催化剂的催化效果与其用量________![]() 填“有关”“无关”或“无法确定”
填“有关”“无关”或“无法确定”![]() 。
。