题目内容
【题目】脱除工业废气中的氮氧化物(主要是指NO和NO2)可以净化空气、改善环境,是环境保护的主要课题。
(1)早期是利用NH3还原法,可将NOx还原为N2进行脱除。
已知:①4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-905.9kJ·mol-1
4NO(g)+6H2O(g) ΔH=-905.9kJ·mol-1
②N2(g)+O2(g)![]() 2NO(g) ΔH=+180kJ·mol-1
2NO(g) ΔH=+180kJ·mol-1
③H2O(g)![]() H2O(l) ΔH=-44kJ·mol-1
H2O(l) ΔH=-44kJ·mol-1
写出常温下,NH3还原NO反应的热化学方程式__。
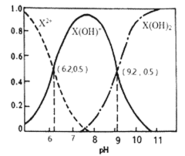
(2)以漂粉精溶液为吸收剂可以有效脱除烟气中的NO。
①漂粉精溶液的主要成分是Ca(ClO)2,若吸收过程中,消耗的Ca(ClO)2与吸收的NO的物质的量之比为3∶4,则脱除后NO转化为__。
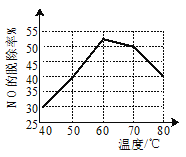
②某一兴趣小组研究不同温度下相同浓度漂粉精溶液对NO脱除率的影响,结果如图所示。图中,40~60℃NO脱除率上升可能的原因为__;60~80℃NO脱除率下降可能的原因为__。
(3)过硫酸钠(Na2S2O8)氧化去除NO
第一步:NO在碱性环境中被Na2S2O8氧化为NaNO2
第二步:NaNO2继续被氧化为NaNO3,反应为![]() +
+![]() +2OH-
+2OH-![]()
![]() +2
+2![]() +H2O。
+H2O。
不同温度下,平衡时![]() 的脱除率与过硫酸钠(Na2S2O8)初始浓度(指第二步反应的初始浓度)的关系如图所示。
的脱除率与过硫酸钠(Na2S2O8)初始浓度(指第二步反应的初始浓度)的关系如图所示。
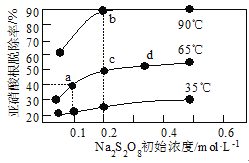
①a、b、c、d四点平衡常数K由大到小的顺序为__,原因是__。
②若a点(0.1,40%)时,![]() 的初始浓度为amol·L-1,平衡时pH=13,则65℃时,第二步反应的平衡常数K=__。(用含a的代数式表示,已知65℃时Kw=1.0×10-13)
的初始浓度为amol·L-1,平衡时pH=13,则65℃时,第二步反应的平衡常数K=__。(用含a的代数式表示,已知65℃时Kw=1.0×10-13)
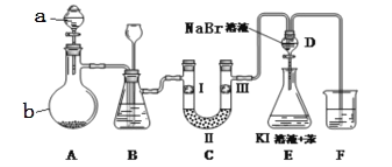
(4)利用新型材料光催化脱除NO法如图所示。
某电化学小组将过程A、B设计成酸性电解池反应,则该反应中阴极反应方程式为___。
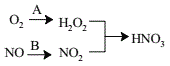
【答案】4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l) ΔH=-2069.9kJmol-1 HNO3(或NO
5N2(g)+6H2O(l) ΔH=-2069.9kJmol-1 HNO3(或NO![]() ) 温度升高,化学反应速率加快,有利于NO充分反应 温度升高,气体溶解度下降;(或温度升高,ClO-水解增强,HClO发生分解等) Kb>Ka=Kc=Kd a、c、d三点在同一温度下,K值相同;b点温度升高,NO
) 温度升高,化学反应速率加快,有利于NO充分反应 温度升高,气体溶解度下降;(或温度升高,ClO-水解增强,HClO发生分解等) Kb>Ka=Kc=Kd a、c、d三点在同一温度下,K值相同;b点温度升高,NO![]() 的脱除率上升,说明平衡向正向移动,K值增大
的脱除率上升,说明平衡向正向移动,K值增大 ![]() O2+2e-+2H+=H2O2
O2+2e-+2H+=H2O2
【解析】
利用盖斯定律,将已知热化学方程式调整化学计量数进行相加减,便可得到待求热化学反应方程式;Ca(ClO)2与吸收的NO的物质的量之比为3∶4,利用得失电子守恒,便可求出含N产物的存在形式。温度升高,NO的脱除率提高,应由温度升高引起;温度继续升高,NO脱除率反而降低,则必存在副反应,且温度升高有利于副反应的发生。化学平衡常数受温度变化的影响,温度相同时,平衡常数不变;升高温度,平衡正向移动,则K值增大。求平衡常数时,可由已知数据,建立三段式,代入公式便可求出K值。设计原电池时,正极O2→H2O2,则电极反应式为O2得电子产物与H+反应生成H2O2。
(1)①4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-905.9kJ·mol-1
4NO(g)+6H2O(g) ΔH=-905.9kJ·mol-1
②N2(g)+O2(g)![]() 2NO(g) ΔH=+180kJ·mol-1
2NO(g) ΔH=+180kJ·mol-1
③H2O(g)![]() H2O(l) ΔH=-44kJ·mol-1
H2O(l) ΔH=-44kJ·mol-1
将①-②×5+③×6得:4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l) ΔH=-2069.9kJmol-1。答案为:4NH3(g)+6NO(g)
5N2(g)+6H2O(l) ΔH=-2069.9kJmol-1。答案为:4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l) ΔH=-2069.9kJmol-1;
5N2(g)+6H2O(l) ΔH=-2069.9kJmol-1;
(2) ①发生反应时,Ca(ClO)2中的Cl由+1价降为-1价,则NO失电子后所得产物中N的价态为![]() =5,从而得出脱除后NO转化为HNO3(或
=5,从而得出脱除后NO转化为HNO3(或![]() )。答案为:HNO3(或
)。答案为:HNO3(或![]() );
);
②图中,40~60℃时,随温度的升高,NO脱除率上升,显然温度升高有利于反应的进行,可能的原因为温度升高,化学反应速率加快,有利于NO充分反应;60~80℃时,温度升高,NO脱除率下降,则应为反应物浓度的下降等,所以可能的原因为温度升高,气体溶解度下降;(或温度升高,ClO-水解增强,HClO发生分解等)。答案为:温度升高,化学反应速率加快,有利于NO充分反应;温度升高,气体溶解度下降;(或温度升高,ClO-水解增强,HClO发生分解等);
(3)①a、c、d三点温度相同,平衡常数相等,b点时温度高,亚硝酸根脱除率大,则表明温度升高平衡正向移动,K值增大,则平衡常数K由大到小的顺序为Kb>Ka=Kc=Kd,原因是a、c、d三点在同一温度下,K值相同;b点温度升高,![]() 的脱除率上升,说明平衡向正向移动,K值增大。答案为:Kb>Ka=Kc=Kd;a、c、d三点在同一温度下,K值相同;b点温度升高,
的脱除率上升,说明平衡向正向移动,K值增大。答案为:Kb>Ka=Kc=Kd;a、c、d三点在同一温度下,K值相同;b点温度升高,![]() 的脱除率上升,说明平衡向正向移动,K值增大;
的脱除率上升,说明平衡向正向移动,K值增大;
②pH=13,65℃时Kw=1.0×10-13,则c(OH-)=1mol/L,利用题给数据,可建立如下三段式:

65℃时,第二步反应的平衡常数K=![]() =
=![]() 。答案为:
。答案为:![]() ;
;
(4)某电化学小组将过程A、B设计成酸性电解池反应,则该反应中阴极为过程A中O2得电子的产物与H+作用生成H2O2,反应方程式为O2+2e-+2H+=H2O2。答案为:O2+2e-+2H+=H2O2。

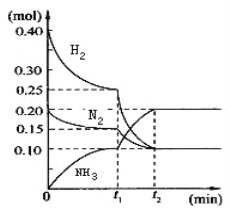
【题目】温度为T1时,向容积为2 L 的密闭容器甲、乙中分别充入一定量的CO(g)和H2O(g),发生反应:CO(g) + H2O(g) ![]() CO2(g) + H2(g) H = -41 kJ/mol。数据如下,下列说法不正确的是
CO2(g) + H2(g) H = -41 kJ/mol。数据如下,下列说法不正确的是
容器 | 甲 | 乙 | ||
反应物 | CO | H2O | CO | H2O |
起始时物质的量(mol) | 1.2 | 0.6 | 2.4 | 1.2 |
平衡时物质的量(mol) | 0.8 | 0.2 | a | b |
A. 甲容器中,平衡时,反应放出的热量为16.4 kJ
B. T1时,反应的平衡常数K甲 = 1
C. 平衡时,乙中CO的浓度是甲中的2倍
D. 乙容器中,平衡时CO的转化率约为75%