题目内容
20.如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )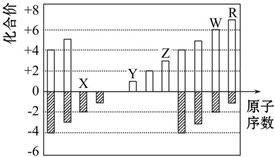
| A. | 原子半径:Z>Y>X | |
| B. | 气态氢化物的稳定性:R<W | |
| C. | WX2和水反应形成的化合物是一种强酸 | |
| D. | Y和Z两者最高价氧化物对应的水化物能相互反应 |
分析 均为短周期元素,由图中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+1价,处于IA族,原子序数大于O元素,故Y为Na元素;Z为+3价,原子序数大于Na,故Z为Al元素;W的化合价为+6、-2价,故W为S元素;R的最高正价为+7价,则R为Cl元素,据此解答.
解答 解:均为短周期元素,由图中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+1价,处于IA族,原子序数大于O元素,故Y为Na元素;Z为+3价,原子序数大于Na,故Z为Al元素;W的化合价为+6、-2价,故W为S元素;R的最高正价为+7价,则R为Cl元素.
A.同周期自左而右原子半径增大、同主族自上而下原子半径减小,故原子半径:Na>Al>O,故A错误;
B.非金属性S<Cl,故氢化物稳定性HCl>H2S,故B错误;
C.SO2和水反应形成的化合物是亚硫酸,亚硫酸属于弱酸,故C错误;
D.Y和Z两者最高价氧化物对应的水化物分别为NaOH、氢氧化铝,二者反应生成偏铝酸钠与水,故D正确,
故选D.
点评 本题考查结构性质与位置关系等,难度不大,根据化合价推断元素是解题的关键,注意对元素周期律的理解掌握.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
9.苯分子中六个碳-碳键是完全等同的,不是单双键交替结构,下列事实可以作为证据的是( )
①苯不能使溴的CCl4溶液褪色;②苯不能使酸性高锰酸钾溶液褪色;③苯在一定条件下既能发生取代反应,又能发生加成反应;④经测定,邻二甲苯只有一种结构;⑤苯的一氯代物只有一种.
①苯不能使溴的CCl4溶液褪色;②苯不能使酸性高锰酸钾溶液褪色;③苯在一定条件下既能发生取代反应,又能发生加成反应;④经测定,邻二甲苯只有一种结构;⑤苯的一氯代物只有一种.
| A. | ①②④⑤ | B. | ①②③⑤ | C. | ①②④ | D. | ①②③④ |
10.分子晶体的熔点通常都在200℃以下,下列数据是对应物质的熔点:据此做出的下列判断中正确的是
( )
| 物质 | Na2O | NaCl | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 熔点/℃ | 920 | 801 | 1291 | 190 | -107 | 2073 | -57 | 1723 |
| A. | NaCl晶体熔化时,吸收的热量用于破坏离子键 | |
| B. | 表中只有BCl3和干冰是分子晶体 | |
| C. | 碳和硅是同一主族,故CO2和 SiO2的晶体类型相同 | |
| D. | 两种含钠化合物是离子晶体,三种含铝化合物也是离子晶体 |
15.硫和硒(Se)、磷(Te)为同主族元素,在生产、生活中有着广泛用途.
Ⅰ、SO2、CO2转化利用是净化环境,造福人类的有效途径,一种用电化学原理,将SO2、CO2转化成用途广泛的化工产品H2SO4和CH3OH,其装置如图所示:

(1)该装置的工作原理是原电池;(填“原电池”或“电解池”)
(2)若A为CO2,B为H2,C为CH3OH,则通入H2-极为负;
(3)若A为SO2,B为O2,C为H2SO4,则A极的电极反应式为SO2+2H2O-2e-=SO42-+4H+.
Ⅱ、硒是地壳中稀有元素,工业上硒鼓废料(主要成分:硒、碲、碳、铜、铁合金)回收精炼硒的一种工艺流程如下:
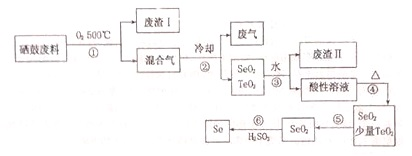
已知:
(1)硒的最高价氧化物对应水化合物化学式:H2SeO4;
(2)废气主要成分是CO2;
(3)步骤④的反应方程式:H2SeO3△_SeO2+H2O;步骤⑥的反应方程式:2H2SO3+SeO2=Se+2H2SO4;
(4)根据表中数据,步骤⑤中分离SeO2和TeO2的最佳方案是升华,将温度控制在315℃到450℃之间.
Ⅰ、SO2、CO2转化利用是净化环境,造福人类的有效途径,一种用电化学原理,将SO2、CO2转化成用途广泛的化工产品H2SO4和CH3OH,其装置如图所示:

(1)该装置的工作原理是原电池;(填“原电池”或“电解池”)
(2)若A为CO2,B为H2,C为CH3OH,则通入H2-极为负;
(3)若A为SO2,B为O2,C为H2SO4,则A极的电极反应式为SO2+2H2O-2e-=SO42-+4H+.
Ⅱ、硒是地壳中稀有元素,工业上硒鼓废料(主要成分:硒、碲、碳、铜、铁合金)回收精炼硒的一种工艺流程如下:

已知:
| 物理性质 | 熔点 | 沸点 | 升华 | 溶解性 |
| SeO2 | 340℃ | 684℃ | 315℃ | 易溶于水 |
| TeO2 | 733℃ | 1260℃ | 450℃ | 易溶于水 |
(2)废气主要成分是CO2;
(3)步骤④的反应方程式:H2SeO3△_SeO2+H2O;步骤⑥的反应方程式:2H2SO3+SeO2=Se+2H2SO4;
(4)根据表中数据,步骤⑤中分离SeO2和TeO2的最佳方案是升华,将温度控制在315℃到450℃之间.
5.下列物质中既存在离子键,又存在共价键的是( )
| A. | Na2O | B. | H2O | C. | HCl | D. | NaOH |
12.草酸是二元中强酸,草酸氢钠溶液显酸性.常温下,向10mL 0.01mol/L NaHC2O4溶液中滴加0.01mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是( )
| A. | V(NaOH)=0时,c(H+)=1×10-2 mol/L | |
| B. | V(NaOH)<10 mL时,可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) | |
| C. | V(NaOH)=10mL时,c(H+)=1×10-7 mol/L | |
| D. | V(NaOH)>10 mL时,c(Na+)>c(HC2O4-)>c(C2O42-) |
10.短周期元素X、Y、Z、W的原子序数依次增大,X 原子的最外层电子数是其内层电子总数的3 倍,Y 原子的最外层只有2 个电子,Z 单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是( )
| A. | 元素W 的简单气态氢化物的热稳定性比X 的强 | |
| B. | 元素W 的最高价氧化物对应水化物的酸性比Z 的弱 | |
| C. | 化合物YX、ZX2、WX3 中化学键的类型相同 | |
| D. | 原子半径的大小顺序:rY>rZ>rW>rX |
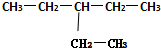 系统命名法:3-乙基戊烷
系统命名法:3-乙基戊烷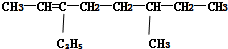 系统命名法:6-甲基-3-乙基-2-辛烯
系统命名法:6-甲基-3-乙基-2-辛烯