��Ŀ����
4���������H��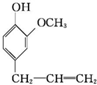 �����������ƿ���ܰ���㾫�Լ����춡��Ӻ������صȣ��ϳɶ�����ӵ�һ��·�����£�
�����������ƿ���ܰ���㾫�Լ����춡��Ӻ������صȣ��ϳɶ�����ӵ�һ��·�����£�
��֪��
��
 ��X����±��ԭ�ӣ���
��X����±��ԭ�ӣ�����A��B��Է�������֮��Ϊ14��E��F��Է�������֮��Ϊ63��
��E���ܷ���������Ӧ��������ˮ�������Ʒ�Ӧ��
��̼̼˫���ϲ������ǻ���
�ݶ������H������ͬ���칹��G�����Ƶã�
�ش��������⣺
��1�������йض�����ӵ�˵������ȷ����AC��
A����FeCl3��Һ��������ɫ B���ɷ���������Ӧ��������Ӧ
C�������巢��ȡ���ͼӳɷ�Ӧ D��1mol��������������3molH2��Ӧ
��2��A�Ĺ���������Ϊ�ǻ���A����B�Ļ�ѧ����ʽΪ
 ��
����3��C����D�ķ�Ӧ����Ϊȡ����Ӧ��D����E�ķ�Ӧ������NaOH��ˮ��Һ�����ȣ�
��4��E����F�Ļ�ѧ����ʽΪCH2=CHCH2OH+HBr$\stackrel{��}{��}$CH2=CHCH2Br+H2O��
��5��G�Ľṹ��ʽΪ
 ��
����6��д���붡����ӻ�Ϊͬ���칹�����������������Ľṹ��ʽ��
 ��
�������ڷ����廯����ں˴Ź���������5��壬�ҷ������Ϊ6��2��2��1��1��
���ܷ���������Ӧ��ˮ�ⷴӦ��
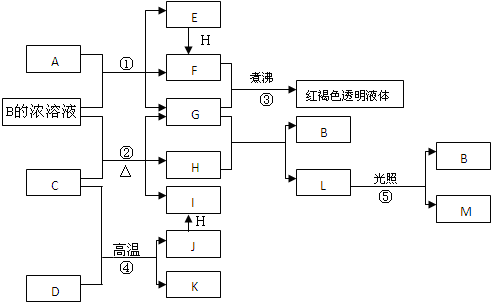
���� A��B��Է�������֮��Ϊ14������A������Ϣ���еķ�Ӧ����BΪ ���������и�����ת����ϵ���H�Ľṹ��ʽ��֪��C����������ȡ����Ӧ����DΪCH2=CHCH2Cl��D��������ˮ���EΪCH2=CHCH2OH��E��F��Է�������֮��Ϊ63������E���廯�ⷢ��ȡ������FΪCH2=CHCH2Br��B��F������Ϣ���еķ�Ӧ����GΪ
���������и�����ת����ϵ���H�Ľṹ��ʽ��֪��C����������ȡ����Ӧ����DΪCH2=CHCH2Cl��D��������ˮ���EΪCH2=CHCH2OH��E��F��Է�������֮��Ϊ63������E���廯�ⷢ��ȡ������FΪCH2=CHCH2Br��B��F������Ϣ���еķ�Ӧ����GΪ ��G�ٷ������ŵ�H���ݴ˴��⣮
��G�ٷ������ŵ�H���ݴ˴��⣮
��� �⣺A��B��Է�������֮��Ϊ14������A������Ϣ���еķ�Ӧ����BΪ ���������и�����ת����ϵ���H�Ľṹ��ʽ��֪��C����������ȡ����Ӧ����DΪCH2=CHCH2Cl��D��������ˮ���EΪCH2=CHCH2OH��E��F��Է�������֮��Ϊ63������E���廯�ⷢ��ȡ������FΪCH2=CHCH2Br��B��F������Ϣ���еķ�Ӧ����GΪ
���������и�����ת����ϵ���H�Ľṹ��ʽ��֪��C����������ȡ����Ӧ����DΪCH2=CHCH2Cl��D��������ˮ���EΪCH2=CHCH2OH��E��F��Է�������֮��Ϊ63������E���廯�ⷢ��ȡ������FΪCH2=CHCH2Br��B��F������Ϣ���еķ�Ӧ����GΪ ��G�ٷ������ŵ�H��
��G�ٷ������ŵ�H��
��1���йض�����ӵ�˵����
A�����ݶ�����ӵĽṹ��ʽ��֪���������з��ǻ���������FeCl3��Һ��������ɫ����A��ȷ��
B��������ӷ�����û��ȩ�������ܷ���������Ӧ����B����
C��������ӷ������б�����̼̼˫���������巢��ȡ���ͼӳɷ�Ӧ����C��ȷ��
D�����ݶ�����ӵĽṹ��ʽ��֪��1mol��������������4molH2������D����
��ѡAC��
��2������A�Ľṹ��ʽ��֪��A�Ĺ���������Ϊ �ǻ���A����B�Ļ�ѧ����ʽΪ  ��
��
�ʴ𰸣��ǻ��� ��
��
��3����������ķ�����֪��C����D�ķ�Ӧ����Ϊȡ����Ӧ��D����±�����ļ���ˮ���E������D����E�ķ�Ӧ������NaOH��ˮ��Һ�����ȣ�
�ʴ�Ϊ��ȡ����Ӧ��NaOH��ˮ��Һ�����ȣ�
��4��E����F�Ļ�ѧ����ʽΪ CH2=CHCH2OH+HBr$\stackrel{��}{��}$CH2=CHCH2Br+H2O��
�ʴ�Ϊ��CH2=CHCH2OH+HBr$\stackrel{��}{��}$CH2=CHCH2Br+H2O��
��5����������ķ�����֪��G�Ľṹ��ʽΪ  ��
��
�ʴ�Ϊ�� ��
��
��6�����������������ڷ����廯������б������ں˴Ź���������5��壬�ҷ������Ϊ6��2��2��1��1�����ܷ���������Ӧ��ˮ�ⷴӦ��˵���м���ij��������������Ķ�����ӵ�ͬ���칹��Ϊ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л�����ƶ������ʣ��漰�л���Ľṹ�����ʣ�Ϊ�߿��������ͣ�������ѧ���ķ��������Ŀ��飬ע������л���Ľṹ�ص�����ŵ����ʣ��ѶȲ���

 ������ҵ����ν�����������ϵ�д�
������ҵ����ν�����������ϵ�д�| A�� | MgO$\stackrel{HCl��ag��}{��}$MgCl2��ag��$\stackrel{��}{��}$��ˮMgCl2 | |
| B�� | Al2O3$\stackrel{NaOH��ag��}{��}$NaAlO2��ag��$\stackrel{HCl��ag��}{��}$AlCl3 | |
| C�� | Fe$\stackrel{Cl_{2}}{��}$FeCl2$\stackrel{Cl_{2}}{��}$FeCl3 | |
| D�� | Cu$\stackrel{ϡHNO_{3}}{��}$NO2$\stackrel{H_{2}O}{��}$NO |
| A�� | A��ƽ����Ӧ����Ϊ 0.1 mol/��L•min�� | |
| B�� | ƽ��ʱ��C��Ũ��Ϊ 0.125 mol/L | |
| C�� | ƽ��ʱ��B��ת����Ϊ 20% | |
| D�� | ƽ��ʱ��������ѹǿΪԭ���� 0.8 �� |
| A�� | ��NH4��2 SO4 | B�� | Al��OH��3 | C�� | NaHSO4 | D�� | Mg��NO3��2 |
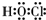 ����Ӧ�ڵĻ�ѧ����ʽΪPbO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$PbCl2+Cl2��+2H2O��
����Ӧ�ڵĻ�ѧ����ʽΪPbO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$PbCl2+Cl2��+2H2O��