题目内容
14.下列物质转化在给定的条件能实现的是( )| A. | MgO$\stackrel{HCl(ag)}{→}$MgCl2(ag)$\stackrel{△}{→}$无水MgCl2 | |
| B. | Al2O3$\stackrel{NaOH(ag)}{→}$NaAlO2(ag)$\stackrel{HCl(ag)}{→}$AlCl3 | |
| C. | Fe$\stackrel{Cl_{2}}{→}$FeCl2$\stackrel{Cl_{2}}{→}$FeCl3 | |
| D. | Cu$\stackrel{稀HNO_{3}}{→}$NO2$\stackrel{H_{2}O}{→}$NO |
分析 A.氯化镁溶液蒸干不能得到氯化镁;
B.氧化铝与NaOH反应生成偏铝酸钠,偏铝酸钠与过量盐酸反应生成氯化铝;
C.Fe与氯气反应只生成氯化铁;
D.Cu与稀硝酸反应生成NO.
解答 解:A.氯化镁溶液蒸干不能得到氯化镁,应为MgO$\stackrel{HCl(ag)}{→}$MgCl2(ag)$→_{△}^{HCl气流}$无水MgCl2,要抑制镁离子水解,故A错误;
B.氧化铝与NaOH反应生成偏铝酸钠,偏铝酸钠与过量盐酸反应生成氯化铝,则Al2O3$\stackrel{NaOH(ag)}{→}$NaAlO2(ag)$\stackrel{HCl(ag)}{→}$AlCl3可实现,故B正确;
C.Fe与氯气反应只生成氯化铁,应为Fe$\stackrel{Cl_{2}}{→}$FeCl3,故C错误;
D.Cu与稀硝酸反应生成NO,应为Cu$\stackrel{稀HNO_{3}}{→}$NO,故D错误;
故选B.
点评 本题考查常见金属及化合物的性质,为高频考点,侧重于学生的分析、应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.

练习册系列答案
相关题目
4.下列各组离子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式正确的是( )
| 选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
| A | Fe2+、NO${\;}_{3}^{-}$、NH${\;}_{4}^{+}$ | NaHSO4溶液 | 3Fe${\;}^{2{+}_{\;}^{\;}}$+NO${\;}_{3}^{-}$+4H+═3Fe3++NO↑+2H2O |
| B | Ca2+、HCO${\;}_{3}^{-}$、Cl- | 少量NaOH溶液 | Ca2++2HCO${\;}_{3}^{-}$+2OH-═2H2O+CaCO3↓+CO${\;}_{3}^{2-}$ |
| C | K+、AlO${\;}_{2}^{-}$、HCO${\;}_{3}^{-}$ | 通入少量CO2 | 2AlO${\;}_{2}^{-}$+3H2O+CO2═2Al(OH)3↓+CO${\;}_{3}^{2-}$ |
| D | NH${\;}_{4}^{+}$、Al3+、SO${\;}_{4}^{2-}$ | 少量Ba(OH)2溶液 | 2NH${\;}_{4}^{+}$+SO${\;}_{4}^{2-}$+Ba2++2OH-═BaSO4↓+2NH3.H2O |
| A. | A | B. | B | C. | C | D. | D |
5.1.024×1023个水分子的物质的是( )
| A. | 0.3 mol | B. | 0.1 mol | C. | 0.2 mol | D. | 2 mol |
9.下列叙述中正确的是( )
| A. | 常温常压下,含有NA个原子的氦气体积约为22.4L | |
| B. | 常温常压下,O2和O3的混合物16g中约含有6.02×1023个氧原子 | |
| C. | 6.4g SO2中含有的原子数为0.2NA | |
| D. | 等体积、等物质的量浓度的强酸中所含的H+数一定相等 |
6.下列说法正确的是( )
| A. | HCl属于共价化合物,溶于水能电离出H+和Cl- | |
| B. | NaOH是离子化合物,该物质中只含离子键 | |
| C. | HI气体受热分解的过程中,只需克服分子间作用力 | |
| D. | 石英和干冰均为原子晶体 |
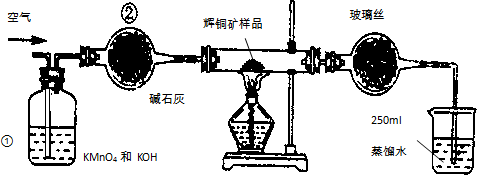
3. 工业上为了测定辉铜矿(主要成分是Cu2S)中Cu2S的质量分数,设计了如图装置.实验时按如下步骤操作:
工业上为了测定辉铜矿(主要成分是Cu2S)中Cu2S的质量分数,设计了如图装置.实验时按如下步骤操作:
A.连接全部仪器,使其成为如图装置,并检查装置的气密性.
B.称取研细的辉铜矿样品1.000g.
C.将称量好的样品小心地放入硬质玻璃管中.
D.以每分钟1L的速率鼓入空气.
E.将硬质玻璃管中的辉铜矿样品加热到一定温度,发生反应为:Cu2S+O2═SO2+2Cu.
F.移取25.00ml含SO2的水溶液于250ml锥形瓶中,用0.0100mol/L KMnO4标准溶液滴定至终点.按上述操作方法重复滴定2-3次.
试回答下列问题:
(1)装置①的作用是除去空气中可能含有的SO2等气体;装置②的作用是干燥气体.
(2)假定辉铜矿中的硫全部转化为SO2,并且全部被水吸收,则操作F中所发生反应的化学方程式为2KMnO4+5H2SO3=2MnSO4+K2SO4+2H2SO4+3H2O;
(3)若操作F的滴定结果如表所示,则辉铜矿样品中Cu2S的质量分数是80%.
(4)本方案设计中有一个明显的缺陷影响了测定结果(不属于操作失误),你认为是(写一种即可):在KMnO4滴定前,未反应完的O2与空气中的O2也可将H2SO3氧化,造成测定结果偏低.
(5)已知在常温下FeS 的Ksp=6.25×10-18,H2S 饱和溶液中c(H+)与c(S${\;}_{2}^{-}$)之间存在如下关系:c2(H+)•c(S2-)=1.0×10-22.在该温度下,将适量 FeS 投入硫化氢饱和溶液中,欲使溶液中(Fe2+)为 lmol/L,应调节溶液的c(H+)为4×10-3mol/L.
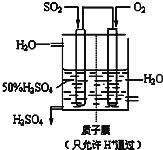
(6)某人设想以如图所示装置用电化学原理生产硫酸,写出通入SO2的电极的电极反应式SO2-2e-+2H2O=SO42-+4H+.
 工业上为了测定辉铜矿(主要成分是Cu2S)中Cu2S的质量分数,设计了如图装置.实验时按如下步骤操作:
工业上为了测定辉铜矿(主要成分是Cu2S)中Cu2S的质量分数,设计了如图装置.实验时按如下步骤操作:A.连接全部仪器,使其成为如图装置,并检查装置的气密性.
B.称取研细的辉铜矿样品1.000g.
C.将称量好的样品小心地放入硬质玻璃管中.
D.以每分钟1L的速率鼓入空气.
E.将硬质玻璃管中的辉铜矿样品加热到一定温度,发生反应为:Cu2S+O2═SO2+2Cu.
F.移取25.00ml含SO2的水溶液于250ml锥形瓶中,用0.0100mol/L KMnO4标准溶液滴定至终点.按上述操作方法重复滴定2-3次.

试回答下列问题:
(1)装置①的作用是除去空气中可能含有的SO2等气体;装置②的作用是干燥气体.
(2)假定辉铜矿中的硫全部转化为SO2,并且全部被水吸收,则操作F中所发生反应的化学方程式为2KMnO4+5H2SO3=2MnSO4+K2SO4+2H2SO4+3H2O;
(3)若操作F的滴定结果如表所示,则辉铜矿样品中Cu2S的质量分数是80%.
| 滴定 次数 | 待测溶液的 体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.04 | 21.03 |
| 2 | 25.00 | 1.98 | 21.99 |
| 3 | 25.00 | 3.20 | 21.24 |
(5)已知在常温下FeS 的Ksp=6.25×10-18,H2S 饱和溶液中c(H+)与c(S${\;}_{2}^{-}$)之间存在如下关系:c2(H+)•c(S2-)=1.0×10-22.在该温度下,将适量 FeS 投入硫化氢饱和溶液中,欲使溶液中(Fe2+)为 lmol/L,应调节溶液的c(H+)为4×10-3mol/L.
(6)某人设想以如图所示装置用电化学原理生产硫酸,写出通入SO2的电极的电极反应式SO2-2e-+2H2O=SO42-+4H+.
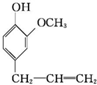 )可用于配制康乃馨型香精以及制异丁香酚和香兰素等,合成丁子香酚的一种路线如下:
)可用于配制康乃馨型香精以及制异丁香酚和香兰素等,合成丁子香酚的一种路线如下:
 (X代表卤素原子);
(X代表卤素原子); .
. .
. .
.