题目内容
下列依据相关实验得出的结论正确的是( )
| 选项 | 实验步骤 | 现象 | 结论 |
| A | 浓硫酸与乙醇加热,产生的气体X直接通入溴水 | 溴水褪色 | X一定是纯净的乙烯 |
| B | 溴乙烷、乙醇及固体NaOH混合加热,产生的气态物质Y,直接通入酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色 | Y一定是纯净的乙烯 |
| C | 在含有酚酞的Na2CO3溶液中加入适量BaCl2溶液振荡 | 红色褪去 | 说明Na2CO3溶液中存在水解平衡 |
| D | Z、W两试管中分别盛有pH和体积相同的盐酸和醋酸溶液,同时分别投入质量大小、形状相同的少量锌粒 | Z中产生气体速率快 | Z中盛放的是盐酸 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.浓硫酸与乙醇加热,可生成乙烯、二氧化硫等气体;
B.乙醇可与酸性高锰酸钾发生氧化还原反应;
C.Na2CO3溶液呈碱性,可使酚酞试液变红,结合影响平衡移动的因素分析;
D.醋酸为弱酸,pH相同时,醋酸浓度较大.
B.乙醇可与酸性高锰酸钾发生氧化还原反应;
C.Na2CO3溶液呈碱性,可使酚酞试液变红,结合影响平衡移动的因素分析;
D.醋酸为弱酸,pH相同时,醋酸浓度较大.
解答:
解:A.浓硫酸与乙醇加热,可生成乙烯,同时浓硫酸与乙醇发生作用可生成二氧化硫等气体,故A错误;
B.乙醇可与酸性高锰酸钾发生氧化还原反应,应先除去乙醇,故B错误;
C.Na2CO3溶液呈碱性,可使酚酞试液变红,加入BaCl2溶液生成碳酸钡沉淀,水解平衡向逆反应方向移动,溶液pH减小,故C正确;
D.醋酸为弱酸,pH相同时,醋酸浓度较大,醋酸反应较快,故D错误.
故选C.
B.乙醇可与酸性高锰酸钾发生氧化还原反应,应先除去乙醇,故B错误;
C.Na2CO3溶液呈碱性,可使酚酞试液变红,加入BaCl2溶液生成碳酸钡沉淀,水解平衡向逆反应方向移动,溶液pH减小,故C正确;
D.醋酸为弱酸,pH相同时,醋酸浓度较大,醋酸反应较快,故D错误.
故选C.
点评:本题考查物质的检验以及性质探究,综合考查学生的分析能力、实验能力和评价能力,为高考常见题型,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度不大.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目
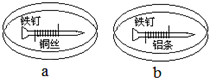 如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是( )
如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是( )| A、a中铁钉附近呈现红色 |
| B、b中铝条附近有气泡产生 |
| C、a中铜丝上发生氧化反应 |
| D、b中铁钉上发生还原反应 |
下列有关实验操作正确的是( )
| A、用Ba(NO3)2溶液可以鉴别SO32-和SO42- |
| B、做H2还原CuO实验时要先通氢气,验纯后再加热 |
C、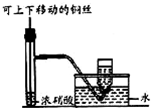 采用如图所示装置可制备并收集少量NO2气体 |
| D、测定相同温度下盐酸和醋酸溶液的pH,就可证明盐酸是强酸、醋酸是弱酸 |
在一定温度下,体积固定的密闭容器中进行可逆反应A(g)+3B(g)?2C(g),下列关于该反应达到平衡状态的标志的说法中不正确的是( )
| A、单位时间内生成n mol A,同时生成3n mol B |
| B、A、B、C的浓度不再发生变化 |
| C、混合气体的压强不再发生改变 |
| D、C生成的速率与C分解的速率相等 |
生活中常用到一些化学知识,下列说法中不正确的是( )
| A、医疗上可用硫酸钡作X射线透视肠胃的内服药,是因为硫酸钡不溶于水 |
| B、未成熟的苹果肉遇碘酒变蓝色,成熟苹果的汁液能与银氨溶液发生反应 |
| C、某雨水样品放置一段时间后pH由4.68变为4.28,是因为水中的亚硫酸逐渐被空气中氧气氧化成硫酸 |
| D、棉花和木材的主要成分都是纤维素,蚕丝和蜘蛛丝的主要成分都是蛋白质 |
下列物质中,可以用于制造半导体的是( )
| A、铝 | B、石墨 |
| C、晶体硅 | D、二氧化硅 |
下列说法中正确的是( )
| A、单质硅是将太阳能转化为电能的常用材料 |
| B、能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 |
| C、原子的最外电子层只有1个电子的元素一定是金属元素 |
| D、光束通过稀豆浆,不会产生丁达尔效应 |
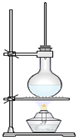 (1)在蔗糖中加入浓H2SO4,反应的化学方程式为
(1)在蔗糖中加入浓H2SO4,反应的化学方程式为