��Ŀ����
13������ʵ�鷽���ܹ��ﵽĿ���ǣ�������| A�� | ����������NaOH��Һ��Ϻ������ã�ֱ����Ӧ��Ļ�����еμ�AgNO3��Һ������Br-�Ĵ��� | |
| B�� | ��������ϡH2SO4��Ϻ���ȣ�3min��4min��ֱ����Ӧ��Ļ�����м���������Һ�����������ǵĴ��ڣ���֪������������������ˮ��������ǣ������Ǻ�ȩ���� | |
| C�� | ���Թ��м���5mL��ˮ��2mL����0.5g���ۣ�������ã��۲��Թܵײ����ɵĺ�ɫ��״Һ�� | |
| D�� | ���Թ��м���Լ2mL������ˮ��Ȼ�����2�Ρ�3�α���ϡ��Һ���۲챽�����巴Ӧ���ɵİ�ɫ���� |
���� A���ڼ���±������±Ԫ��ʱ��Ӧ���Ƚ�±��������ˮ�ⷴӦ��Ȼ��������кͣ����μ���������Һ����±���ӣ�
B����ӦӦ�ڼ��������£�
C��������ˮ����Ӧ��������ȡ�������ܶȱ�ˮС��
D�����Ӻ���ˮ��Ӧ����ȡ����Ӧ��
��� �⣺A�������������е���Ԫ��ʱ��Ӧ���Ƚ����������������ˮ��Һ����ˮ�ⷴӦ�����ƶ��������ӣ�Ȼ��������кͣ����μ���������Һ���������ӣ������������ɫ��������֤��������Ԫ�أ���A����
B����ӦӦ�ڼ��������£�Ӧ�����������к����ʼ��ԣ���B����
C��������ˮ����Ӧ��������ȡ�������ܶȱ�ˮС����ɫҺ�����ϲ㣬��C����
D�����Ӻ��巢��ȡ����Ӧ�������屽�Ӱ�ɫ�������廯�⣬��D��ȷ��
��ѡD��
���� ���⿼���Ϊ�ۺϣ��漰�л���ļ��������ʵȣ�������ѧ���ķ���������ʵ�������Ŀ��飬Ϊ��Ƶ���㣬ע�����ʵ��ķ����������ʹ�õ�������ע����ػ���֪ʶ�Ļ��ۣ��ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
3�����и��������У�������Һ�������ӷ�����ʱð���̣�������������������ǣ�������
| A�� | N2 | B�� | NO | C�� | NH3 | D�� | NO2? |
4��������Ҫ�Ļ���ԭ�ϣ����������صȶ��ֲ�Ʒ��
��1���ϳɰ����õ��������Լ���Ϊԭ���Ƶã��йػ�ѧ��Ӧ�������仯��ͼ1��ʾ��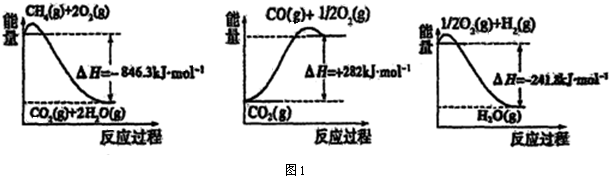
CH4��g����H2O��g����Ӧ����CO��g����H2��g�����Ȼ�ѧ����ʽΪ��CH4��g��+H2O��g��=CO��g��+3H2 ��g����H=+161.1kJ•mol-1��
��2��CO�Ժϳɰ��Ĵ����ж������ã����������������ͭ��Һ������ԭ������CO���䷴Ӧԭ��Ϊ��
[Cu��NH3��2CH3COO]��l��+CO��g��+NH3��g��?[Cu��NH3��3]CH3COO•CO��l������H��0
����CO�������ͭ��Һ�����ʵ��������ֿ��������ָ�������CO�������Թ�ѭ��ʹ�ã�����������������B������дѡ���ţ�
A�����¡���ѹ�� ��B�����¡���ѹ���� C�����¡���ѹ��������D�����¡���ѹ
��3��������ȡ����[CO��NH2��2]�ķ�ӦΪ��2NH3��g��+CO2��g��?CO��NH2��2��1��+H2O��g����H��0��ij�¶��£����ݻ�Ϊ100L���ܱ�������ͨ��4molNH3��2molCO2���÷�Ӧ���е�40sʱ�ﵽƽ�⣬��ʱCO2��ת����Ϊ50%�����¶��´˷�Ӧƽ�ⳣ��KΪ2500L2•mol-2��
��4��ȡ������ͬ�ĺ���������������ͬ�¶ȣ������������CO2���壬����ʵ�����ݻ��Ƴ�c��NH3����ʱ�䣨t���仯��������ͼ2��ʾ����A��B�ֱ�Ϊ��ͬ�¶�ʱ�ⶨ�����ߣ���A���A����B������������Ӧ��ʵ���¶ȸߣ��жϵ�������A������ʼŨ��С������20minʱ���ڷ�Ӧ���ʿ죬˵�����¶ȸߣ�
��5����֪ijЩ���������ˮ�еĵ���ƽ�ⳣ����25�棩���±���
���г�����0.1mol•L-1�ģ�NH4��2CO3��Һ��
�ٸ���Һ�ʼ��ԣ���ᡱ�����С����������ԭ��������NH3•H2O�ĵ���ƽ�ⳣ������HCO3-�ĵ���ƽ�ⳣ�������CO32-ˮ��̶ȴ���NH4+ˮ��̶ȣ���Һ��c��OH-����c��H+������Һ�ʼ��ԣ�
�ڸã�NH4��2CO3��Һ�и���Ũ��֮��Ĺ�ϵʽ����ȷ����B����
A��c��NH4+����c��CO32-����c��HCO3-����c��NH3•H2O��
B��c��NH4+��+c��H+��=c��HCO3-��+c��OH-��+c��CO32-��
C��c��CO32-��+c��HCO3-��+c��H2CO3��=0.1mol•L-1
D��c��NH4+��+c��NH3•H2O��=2c��CO32-��+2c��HCO3-��+2c��H2CO3��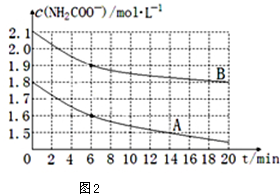
��1���ϳɰ����õ��������Լ���Ϊԭ���Ƶã��йػ�ѧ��Ӧ�������仯��ͼ1��ʾ��

CH4��g����H2O��g����Ӧ����CO��g����H2��g�����Ȼ�ѧ����ʽΪ��CH4��g��+H2O��g��=CO��g��+3H2 ��g����H=+161.1kJ•mol-1��
��2��CO�Ժϳɰ��Ĵ����ж������ã����������������ͭ��Һ������ԭ������CO���䷴Ӧԭ��Ϊ��
[Cu��NH3��2CH3COO]��l��+CO��g��+NH3��g��?[Cu��NH3��3]CH3COO•CO��l������H��0
����CO�������ͭ��Һ�����ʵ��������ֿ��������ָ�������CO�������Թ�ѭ��ʹ�ã�����������������B������дѡ���ţ�
A�����¡���ѹ�� ��B�����¡���ѹ���� C�����¡���ѹ��������D�����¡���ѹ
��3��������ȡ����[CO��NH2��2]�ķ�ӦΪ��2NH3��g��+CO2��g��?CO��NH2��2��1��+H2O��g����H��0��ij�¶��£����ݻ�Ϊ100L���ܱ�������ͨ��4molNH3��2molCO2���÷�Ӧ���е�40sʱ�ﵽƽ�⣬��ʱCO2��ת����Ϊ50%�����¶��´˷�Ӧƽ�ⳣ��KΪ2500L2•mol-2��
��4��ȡ������ͬ�ĺ���������������ͬ�¶ȣ������������CO2���壬����ʵ�����ݻ��Ƴ�c��NH3����ʱ�䣨t���仯��������ͼ2��ʾ����A��B�ֱ�Ϊ��ͬ�¶�ʱ�ⶨ�����ߣ���A���A����B������������Ӧ��ʵ���¶ȸߣ��жϵ�������A������ʼŨ��С������20minʱ���ڷ�Ӧ���ʿ죬˵�����¶ȸߣ�
��5����֪ijЩ���������ˮ�еĵ���ƽ�ⳣ����25�棩���±���
| ������� | H2CO3 | NH3•H2O |
| ����ƽ�ⳣ�� | Ka1=4.30��10-7��������Ka2=5.61��10-11 | Kb=1.77��10-5 |
�ٸ���Һ�ʼ��ԣ���ᡱ�����С����������ԭ��������NH3•H2O�ĵ���ƽ�ⳣ������HCO3-�ĵ���ƽ�ⳣ�������CO32-ˮ��̶ȴ���NH4+ˮ��̶ȣ���Һ��c��OH-����c��H+������Һ�ʼ��ԣ�
�ڸã�NH4��2CO3��Һ�и���Ũ��֮��Ĺ�ϵʽ����ȷ����B����
A��c��NH4+����c��CO32-����c��HCO3-����c��NH3•H2O��
B��c��NH4+��+c��H+��=c��HCO3-��+c��OH-��+c��CO32-��
C��c��CO32-��+c��HCO3-��+c��H2CO3��=0.1mol•L-1
D��c��NH4+��+c��NH3•H2O��=2c��CO32-��+2c��HCO3-��+2c��H2CO3��

8����ij��ѧ��־���������ⷢ����һ���µ����η��ӣ����ķ���ʽΪC60Si60������ӽṹ�����й���ͳ����Ʒ���ε����ⶨ���а���C60��Ҳ��Si60�ṹ��������������ȷ���ǣ�������
| A�� | �����ʵ��۵㲻��ܸߡ�Ӳ�Ȳ���ܴ� | |
| B�� | �������γɵľ������ڷ��Ӿ��� | |
| C�� | �����ʷ�����Si60��������C60���� | |
| D�� | �����ʵ���Է�������Ϊ2400 |
18�����õ��ϴ���������ķ����ǣ�������
| A�� | ��������������ȡ����Ӧ | B�� | ��ϩ�����������ӳɷ�Ӧ | ||
| C�� | ��ϩ���Ȼ��ⷢ���ӳɷ�Ӧ | D�� | ��Ȳ���Ȼ��ⷢ���ӳɷ�Ӧ |
5�����й�����ε���������ȷ���ǣ�������
| A�� | �������ӻ����� | B�� | ���ȶ��ֽܷ������ | ||
| C�� | ��������ˮ | D�� | ��������Ӧ�ų����� |