题目内容
(16分)(1)下列有关实验操作或判断不正确的是 。
| A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏小 |
| B.用干燥的pH试纸测定氯水的pH |
| C.配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌 |
| D.在天平左右两盘中各放一张白纸后,即可将NaOH固体放在白纸上称量 |
F.制备氢氧化亚铁时,将盛有NaOH溶液的滴管,伸入硫酸亚铁溶液中
(2)除杂(括号内为杂质):请把所加试剂和有关离子反应方程式填在空白处。
| | 试剂 | 离子反应方程式 |
| ①NaHCO3溶液(Na2CO3) | | |
| ② Fe2O3(Al2O3) | | |
| ③FeCl3溶液(FeCl2) | | |
| ④CO2(HCl) | | |
(1)A、 B、D、E (4分)
(2)(方程式每个2分,其余每空1分) 试剂 离子反应方程式 ①NaHCO3溶液(Na2CO3) CO2 CO32-+CO2+H2O === 2HCO3- ② Fe2O3(Al2O3) NaOH溶液 Al2O3+2OH-══ 2AlO2-+H2O ③FeCl3溶液(FeCl2) Cl2 2Fe2++ Cl2=2Fe3++ 2Cl- ④CO2(HCl) 饱和的NaHCO3溶液 HCO3-+H+= CO2↑+ H2O
解析试题分析:(1)A.配制一定物质的量浓度溶液,定容时俯视刻度线,溶液的体积偏小,则会导致所配溶液浓度偏大,错误;B.由于氯水中含有强氧化剂HClO,所以试纸先因为含有HCl而变红,或又会被氧化而褪色,因此不能用干燥的pH试纸测定氯水的pH,错误;C.配制稀硫酸时,由于浓硫酸的密度比水大,溶于水会放热,所以可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌,正确;D.由于NaOH有腐蚀性,所以不能在天平上直接称量NaOH,应该在烧杯中进行称量,错误;E.观察钾元素焰色反应的操作:先将铂丝放在稀盐酸中洗涤,然后在酒精灯的火焰上灼烧至于火焰的颜色相近时,再蘸取氯化钾溶液,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃观察,错误。F.制备氢氧化亚铁时,为防止制取的氢氧化亚铁被空气中的氧气氧化,将盛有NaOH溶液的滴管,伸入硫酸亚铁溶液中,正确。(2)①NaHCO3溶液(Na2CO3)应该向溶液中通入CO2,反应的离子方程式是CO32-+CO2+H2O === 2HCO3-;② Fe2O3(Al2O3)利用Al2O3的两性,用NaOH溶液溶解,发生反应:Al2O3+2OH-══ 2AlO2-+H2O,最后过滤即可;③FeCl3溶液含有FeCl2杂质,可利用Fe2+的还原性,用氯气将其氧化除去,反应的方程式是:2Fe2++ Cl2=2Fe3++ 2Cl-;④ CO2中含有HCl杂质气体,可以通过盛有饱和的NaHCO3溶液的洗气瓶来除去,反应的离子方程式是:HCO3-+H+= CO2↑+ H2O。
考点:考查化学实验基本操作的正误判断、杂质的除去时的试剂的选择及离子方程式的书写的知识。

 口算题天天练系列答案
口算题天天练系列答案下列实验操作正确且能达到目的是
| A.将AlCl3溶液蒸发结晶提取无水AlCl3 |
| B.在温水瓶中加入Na2CO3溶液泡浸后加入盐酸能除去内壁CaSO4 |
| C.用饱和的NaOH热溶液除去乙酸乙酯中的乙醇、乙酸 |
| D.将Cl2、HCl混合气体通过盛有NaHCO3饱和溶液的洗气瓶除去HCl |
下列装置不能完成实验的是 ( )
| | 装置 | 实验 | | 装置 | 实验 |
| A |  | 结合秒表测 量锌与硫酸 的反应速率 | C |  | 验证化学能 转化为电能 |
| B |  | 吸收多余 HBr气体 | D |  | 实验室制 取少量乙酸 乙酯 |
下列叙述正确的是( )
①装置甲可防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可验证HCl气体在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤装置戊既可用于收集H2、CO2、Cl2和HCl气体,也可用于干燥H2、CO2、Cl2和HCl气体。
| A.①⑤ | B.④⑤ | C.①② | D.③⑤ |
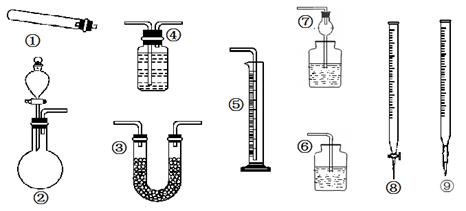
某化学小组的同学到实验室学习。在实验桌上摆有如图所示仪器:
(1)指导教师要求同学们写出仪器的名称,某同学书写的答案如下表,请你找出其中的错误,将改正后的名称填写在下表中(若正确,则此空不需要填写)。
| 仪器编号 | a | b | c | d | e |
| 名称 | 试管 | 溶量瓶 | 集气瓶 | 碱式滴定管 | 普通漏斗 |
| 改正的名称 | | | | | |
(2)甲同学想用d进行实验,请你说出该仪器(已经洗涤干净)使用时的第一步操作: 。
(3)关于e的用途,乙同学说可组成防倒吸装置。你还能说出其他两种用途吗?
① ;
② 。
(4)丙同学想用如图所示装置用大理石和稀盐酸反应制取CO2。老师指出,这需要太多的稀盐酸,会造成浪费,该同学选用了上面的一种仪器,加在装置中,解决了这个问题。请你把该仪器画在图中合适的位置。

工业上以锂辉石(Li2O·Al2O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:
已知:①Li2O·Al2O3·4SiO2 H2SO4(浓)
H2SO4(浓) Li2SO4
Li2SO4 Al2O3·4SiO2·H2O↓
Al2O3·4SiO2·H2O↓
②某些物质的溶解度(S)如下表所示:
| T/℃ | 20 | 40 | 60 | 80 |
 (Li2CO3)/g (Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
 (Li2SO4)/g (Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
③从滤渣1中提取出Si的部分流程如下图所示:

根据以上信息,请回答下列问题:
(1)括号内应提供的相应条件和物质 、 。
(2)方框中所得物质的化学式 。
(3)使用浓硫酸并加热到250℃~300℃的目的是 。
(4)②处加Na2CO3溶液所发生反应的离子方程式 、 。
(5)滤渣2的主要成分有 。
(6)如何检验Li2CO3是否洗涤干净? 。