题目内容
【题目】前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A+无电子,B的最简单气态氢化物能引起温室效应,D原子核外电子有8种不同的运动状态, E是用途最广泛的金属,F元素的基态原子最外能层只有一个电子,其它能层均已充满电子。
(1)E元素在周期表中的位置 ;F+的电子排布式为 。
(2)化合物BD(CA2)2中,B原子的杂化方式为 ,1mol该分子中σ键数目为 个,该物质易溶于水的主要原因是 _ _____________。
(3)ACD3中阴离子CD3-的空间构型为 ,ACD3酸性比ACD2强,原因是___________。
(4)根据等电子体原理,BD分子的电子式为 ,E与BD形成的化合物E(BD)5熔点253K,沸点376K,其固体属于 晶体。
(5)3g B2A6在足量氧气中燃烧并恢复到室温,放出Q kJ热量,则表示B2A6燃烧热的热化学方程式为
______ _ _____________。
(6)将F单质粉末加入到CA3的浓溶液中,并通入D2,充分反应后溶液呈深蓝色,写出该反应的化学方程式 _ _____________。
【答案】
(1)第4周期Ⅷ族(1分) [Ar]3d10(1分)
(2)sp2杂化(1分) 7NA(1分) 与水分子之间能形成氢键(1分)
(3)平面三角形(1分) 非羟基氧个数HNO3比HNO2多(1分)
(4)![]() (1分) 分子(1分)
(1分) 分子(1分)
(5)C2H6(g)+ ![]() O2(g)=2CO2(g)+3H2O(l), ΔH=-10QkJ/mol(2分)
O2(g)=2CO2(g)+3H2O(l), ΔH=-10QkJ/mol(2分)
(6)2Cu+ O2 + 8NH3+ 2H2O =2[Cu(NH3)4](OH)2(2分)
【解析】
试题分析:前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A+无电子,A为H元素;B的最简单气态氢化物能引起温室效应,B为C元素;D原子核外电子有8种不同的运动状态,即有8个电子,D为O元素;则C为N元素;E是用途最广泛的金属,E为Fe元素;F元素的基态原子最外能层只有一个电子,其它能层均已充满电子,F为Cu元素。
(1)Fe元素在周期表中位于第4周期Ⅷ族;Cu+的电子排布式为[Ar]3d10,故答案为:第4周期Ⅷ族;[Ar]3d10;
(2)化合物CO(NH2)2中,C原子连接有三个原子,没有孤对电子,杂化方式为sp2杂化;尿素的结构简式为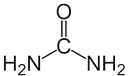 ,1mol该分子中σ键数目为7NA个,该分子与水分子之间能形成氢键,因此该物质易溶于水,故答案为:sp2杂化;7NA;与水分子之间能形成氢键;
,1mol该分子中σ键数目为7NA个,该分子与水分子之间能形成氢键,因此该物质易溶于水,故答案为:sp2杂化;7NA;与水分子之间能形成氢键;
(3)HNO3中阴离子NO3-中N原子上连接3个原子,孤电子对数为![]() (5+1-3×2)=0,采用空间sp2杂化,空间构型为平面三角形,非羟基氧个数HNO3比HNO2多,HNO3酸性比HNO2强,故答案为:平面三角形;非羟基氧个数HNO3比HNO2多;
(5+1-3×2)=0,采用空间sp2杂化,空间构型为平面三角形,非羟基氧个数HNO3比HNO2多,HNO3酸性比HNO2强,故答案为:平面三角形;非羟基氧个数HNO3比HNO2多;
(4)根据原理,CO与N2属于等电子体,分子的电子式为![]() ,化合物的熔点253K,沸点376K,都较低,其固体属于分子晶体,故答案为:
,化合物的熔点253K,沸点376K,都较低,其固体属于分子晶体,故答案为:![]() ;分子;
;分子;
(5)3g C2H6的物质的量为![]() =0.1mol,则1mol燃烧放出10Q kJ热量,则表示B2A6燃烧热的热化学方程式为C2H6(g)+7/2O2(g)=2CO2(g)+3H2O(l), ΔH=-10QkJ/mol,故答案为 C2H6(g)+7/2O2(g) =2CO2(g)+3H2O(l), ΔH=-10QkJ/mol;
=0.1mol,则1mol燃烧放出10Q kJ热量,则表示B2A6燃烧热的热化学方程式为C2H6(g)+7/2O2(g)=2CO2(g)+3H2O(l), ΔH=-10QkJ/mol,故答案为 C2H6(g)+7/2O2(g) =2CO2(g)+3H2O(l), ΔH=-10QkJ/mol;
(6)反应后溶液呈深蓝色,反应生成了铜氨络合物,反应的化学方程式为2Cu+ O2 + 8NH3+ 2H2O =2[Cu(NH3)4](OH)2,故答案为:2Cu+ O2 + 8NH3+ 2H2O =2[Cu(NH3)4](OH)2。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案【题目】Ⅰ.施莱辛(Schlesinger)等人提出可用NaBH4与水反应制取氢气:BH4- + 2H2O == BO2- + 4H2↑(反应实质为水电离出来的H+被还原)。研究表明,该反应生成H2的速率受外界条件影响,下表为pH和温度对NaBH4半衰期的影响(半衰期是指反应过程中,某物质的浓度降低到初始浓度一半时所需的时间)。
体系 pH | 不同温度下的半衰期(min) | |||
0℃ | 25℃ | 50℃ | 75℃ | |
8 | 4.32×100 | 6.19×10-1 | 8.64×10-2 | 1.22×10-2 |
10 | 4.32×102 | 6.19×101 | 8.64×100 | 1.22×100 |
12 | 4.32×104 | 6.19×103 | 8.64×102 | 1.22×102 |
14 | 4.32×106 | 6.19×105 | 8.64×104 | 1.22×104 |
(1)已知NaBH4与水反应后所得溶液显碱性,用离子方程式表示出溶液显碱性的原因 ,溶液中各离子浓度大小关系为 。
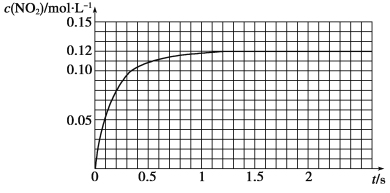
(2)从上表可知,温度对NaBH4与水反应速率产生怎样的影响? 。
(3)反应体系的pH为何会对NaBH4与水反应的反应速率产生影响? 。
Ⅱ.肼(N2H4)又称联氨,常温下是一种无色油状液体,沸点为113.5℃。肼和氧气在不同温度和催化剂条件下生成不同产物(如图)。
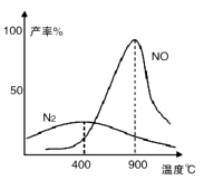
温度较低时主要反应①:N2H4 + O2 ![]() N2 + 2H2O
N2 + 2H2O
温度较高时主要反应②:N2H4 + 2O2 ![]() 2NO + 2H2O
2NO + 2H2O
不考虑其他反应,完成下列填空:
(4)若反应①在250℃时的平衡常数为K1,350℃时的平衡常数为K2,则K1 K2(填“>”、“<”或“=”)。
(5)反应于1100℃时达到平衡后,下列措施能使容器中![]() 增大的有 (填字母序号)。
增大的有 (填字母序号)。
A.恒容条件下,充入He气
B.增大容器体积
C.恒容条件下,充入N2H4
D.使用催化剂
(6)若将n mol肼和2n molO2充入某容积为n L的刚性容器中,在800℃和一定压强、合适催化剂的作用下,反应①和②同时达到平衡,实验测得N2的产率x,NO的产率为y,则该条件下反应②的平衡常数K= (用x、y的代数式表示,不必化简)。