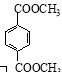
��Ŀ����
����Ŀ���ϳɰ���ҵ�ϳ������з����Ʊ�H2��
�����٣�C��s��+2H2O��g��![]() CO2��g��+2H2��g��
CO2��g��+2H2��g��
�����ڣ�CO��g��+H2O��g��![]() CO2��g��+H2��g��
CO2��g��+H2��g��
��1����֪��C��ʯī��+O2��g���TCO2��g����H=-394kJmol-1
��2C��ʯī��+O2��g���T2CO2��g����H=-222kJmol-1
��2H2��g��+O2��g���T2H2O��g����H=-484kJmol-1
�Լ���25��ʱ�ɷ������Ʊ�1000gH2���ų�������Ϊ______kJ��
��2����һ���������£���C��s����H2O��g���ֱ����ס��������ܱ�������������Ӧ��C��s��+2H2O��g��![]() CO2��g��+2H2��g��������������±���ʾ��
CO2��g��+2H2��g��������������±���ʾ��

��T1______T2�����������=����������T1��ʱ���÷�Ӧ��ƽ�ⳣ��K=______��
���������У�����Ӧ���е�1.5minʱ��H2O��g�������ʵ���Ũ�ȷ�Χ��______��
�����ܱպ��ݵ������У��ܱ�ʾ������Ӧ�ﵽ��ѧƽ��״̬����______��
A��V�棨CO2��=2V����H2��
B�����������ܶȱ��ֲ���
C��c��H2O����c��CO2����c��H2��=2��1��2
D����������ƽ��Ħ���������ֲ���
��ijͬѧΪ���о���Ӧ�����Ի�ѧƽ���Ӱ�죬����淴Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��

��t1��t3��t5��t7ʱ��Ӧ�����˵�ƽ��״̬�����t2��t4��t6��t8ʱ��ֻ�ı���һ����Ӧ��������t6ʱ�̸ı��������________________________����t1��t8�ĸ�ʱ���H2O��g����ƽ��ת�������______��
���𰸡���1��20500kJ��2����>12.8�ڴ���0.8mol/L��С��1.4mol/L��BD �� ͨ��H2O t7-t8
��������
�����������1�����ݸ�˹������CO��g��+H2O��g��![]() CO2��g��+H2��g��������H=��H1-��H2-��H3=-394kJmol-1-��-111kJmol-1��-��-242kJmol-1��=-41kJmol-1�������Ʊ�1000g H2���ų�������Ϊ41��2��1000= 20500kJ��
CO2��g��+H2��g��������H=��H1-��H2-��H3=-394kJmol-1-��-111kJmol-1��-��-242kJmol-1��=-41kJmol-1�������Ʊ�1000g H2���ų�������Ϊ41��2��1000= 20500kJ��
��2������������¶���ȣ�������ң���ƽ��ʱH2��g��ƽ����Ϊ2.4mol��ʵ������3.2��˵���¶ȸı䣬ƽ�������ƶ���������ӦΪ���ȷ�Ӧ������T1��T2��
�ɱ������ݿ�֪��ƽ��ʱ���������ʵ���Ϊ3.2mol����
C��s��+2H20��g��![]() C02��g��+2H2��g��
C02��g��+2H2��g��
��ʼ��mol����2 4 0 0
ת����mol����1.6 3.2 1.6 3.2
ƽ�⣨mol����0.4 0.8 1.6 3.2
ƽ�ⳣ��K=��1.6��3.22����0.82=12.8��
��3min��ˮ������Ũ�ȱ仯��=������Ũ�ȱ仯����=1.2mol��1L=1.2mol/L�����ŷ�Ӧ�Ľ��У����ʵ�Ũ�Ƚ��ͣ���Ӧ���ʱ�С������ǰ1.5minˮ��Ũ�ȱ仯�����ں�1.5minˮ��Ũ�ȱ仯������Ӧ���е�1.5minʱ��H2O��g�������ʵ���Ũ��С��2mol/L-1.2mol/L��1/2=1.4mol/L��ƽ��ʱ��ˮ������Ũ��Ϊ0.8mol/L������H2O��g�������ʵ���Ũ�ȷ�Χ������0.8mol/L��С��1.4mol/L��
��A����V�棨CO2��=2V����H2�����淴Ӧ����֮�Ȳ����ڻ�ѧ������֮�ȣ��������ٶȲ��ȣ���ѡ��B.�ں����ܱ������У����ŷ�Ӧ�Ľ��У����������������p=m��V���ܶ����������������ܶȱ��ֲ���ʱ��˵�������ٶ���ȣ�ѡ��C������������֮���Ũ�ȹ�ϵ����ʼ��������ת�����йأ��뷴Ӧ�Ƿ�ﵽƽ���أ��ʲ�ѡ��D.��������ƽ����Է�������δƽ��ʱ�ڱ䣬���ڱ��ֲ��䣬˵���Ѵ�ƽ��״̬��ѡ����ѡBD��
��t1��t6ƽ�ⶼ�����ƶ�����t6ʱƽ�������ƶ�������Ϊ���ӷ�Ӧ���Ũ�ȣ���C�ǹ��壬������ͨ��ˮ������ͨ��ˮ�����൱������ѹǿ��ƽ�������ƶ���ˮ������ת���ʽ��ͣ�t8ʱ��Ӧ��������ƽ�ⲻ�ƶ�������ƽ��ת�������t7-t8 ��

 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�����Ŀ������п����ΪʳƷпǿ������ԭ�ϡ���ҵ�ϳ�����п����������п����п�����Ҫ�ɷ���ZnCO3������������Fe2O3��FeCO3MgO��CaO�ȣ�������������ͼ���£�

��1������п����ĥ�ɷ۵�Ŀ����_____��
��2����������������������з�Ӧ�����ӷ���ʽ����Fe(OH)2+��____+��_____=��Fe(OH)3+��CI-
��3��������(Goethite)���Ե¹�ʫ�˸��(Goethe)���������ģ����Ԫ����Fe��O��H��Ħ������Ϊ89g/mol����ѧʽ��_______����Al��NiO(OH)Ϊ�缫��NaOH��ҺΪ���Һ���һ�����͵�أ��ŵ�ʱ������ת��ΪFe(OH)2���õ�طŵ練Ӧ�Ļ�ѧ����ʽ��__________��
��4�������±����ݣ���������Һ2����pHʱ�������Ͽ�ѡ�õ��������Ϊ______��
������ѧʽ | Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 |
��ʼ������pH | 10��4 | 6��4 | �� | �� |
������ȫ��pH | 12��4 | 8��0 | �� | �� |
��ʼ�ܽ��pH | �� | 10��5 | �� | �� |
Ksp | 5��6�� | �� | 6��8�� | 2��8�� |
��5����ҵ�ϴ�����Һ3����ȡMgO�����У����ʵķ�Ӧ����______(ѡ�����)��
a������ʯ�� b��ʯ���� c��������Һ d����ˮ
��6������Һ4��֮��IJ�������Ϊ______��_______�����ˣ�ϴ�ӣ����
��7������ͼ�����ݣ���п�����ZnCO3����������������________(�ô���ʽ��ʾ)