题目内容
10.下列反应过程中的能量变化情况符合如图的是( )
| A. | 乙醇的燃烧 | B. | 碳酸钙的分解 | ||
| C. | 镁和盐酸的反应 | D. | 酸和碱的中和反应 |
分析 生成物具有的总能量高于反应物具有的总能量,该反应为吸热反应;常见的吸热反应:C(s)+H2O(g)→CO(g)+H2O; C+CO2→CO的反应,Ba(OH)2•8H2O与NH4Cl的反应以及KClO3、KMnO4、CaCO3的分解等;
解答 解:A.乙醇的燃烧反应是放热反应,故A错误;
B.碳酸钙的分解反应是吸热反应,故B正确;
C.镁和盐酸反应是放热反应属于氧化还原反应放热,故C错误;
D.酸和碱的中和反应是放热反应,故D错误.
故选B.
点评 本题考查化学反应的热量变化,难度不大,学生应注重归纳中学化学中常见的吸热或放热的反应.

练习册系列答案
相关题目
15.下列表示物质结构的化学用语或模型图正确的是( )
| A. | 二氧化碳的电子式: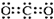 | B. | 14C的原子结构示意图: | ||
| C. | C3H8的结构式CH3-CH2-CH3 | D. | 次氯酸的电子式: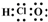 |
1.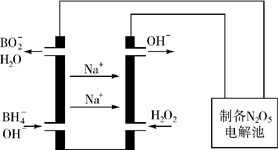 氮的重要化合物如氨、肼(N2H4)、NO、NO2、HNO3、硝酸盐等,在生产、生活中具有重要作用.
氮的重要化合物如氨、肼(N2H4)、NO、NO2、HNO3、硝酸盐等,在生产、生活中具有重要作用.
(1)利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g)△H1=+44.0kJ•mol-1
N2(g)+O2(g)=2NO(g)△H2=+229.3kJ•mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3=-906.5kJ•mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H4,则△H4=-2317.0kJ•mol-1.
(2)亚硝酸是一种弱酸,能证明亚硝酸是弱电解质的是AD
A.常温下,亚硝酸钠溶液的pH>7
B.亚硝酸能和NaOH发生中和反应
C.用亚硝 酸 溶液做导电性实验,灯泡很暗
D.常温下,将pH=3的亚硝酸溶液稀释10倍,pH<4
(3)一定温度下,将a mol/L的氨水与b mol/LH2SO4溶液等体积混合,充分反应后有:2c(SO42-)=c(NH4+),用含a和b的代数式表示该混合溶液中NH3•H2O的电离常数为$\frac{2b}{a-2b}$×10-7.
(4)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体,写出该反应的离子方程式:2Co2++N2H4+4OH-=2Co↓+N2↑+4H2O.
(5)X、Y、Z、W分别是HNO3、NH4NO3、NaOH、NaNO2四种强电解质中的一种.下表是常温下浓度均为0.01mol•L-1的X、Y、Z、W溶液的pH.
将X、Y、Z各1mol同时溶于水中制得混合溶液,则混合溶液中各离子的浓度由大到小的顺序为c(Na+)>c(NO3-)>c(NO2-)>c(OH-)>c(H+).
 氮的重要化合物如氨、肼(N2H4)、NO、NO2、HNO3、硝酸盐等,在生产、生活中具有重要作用.
氮的重要化合物如氨、肼(N2H4)、NO、NO2、HNO3、硝酸盐等,在生产、生活中具有重要作用.(1)利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g)△H1=+44.0kJ•mol-1
N2(g)+O2(g)=2NO(g)△H2=+229.3kJ•mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3=-906.5kJ•mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H4,则△H4=-2317.0kJ•mol-1.
(2)亚硝酸是一种弱酸,能证明亚硝酸是弱电解质的是AD
A.常温下,亚硝酸钠溶液的pH>7
B.亚硝酸能和NaOH发生中和反应
C.用亚硝 酸 溶液做导电性实验,灯泡很暗
D.常温下,将pH=3的亚硝酸溶液稀释10倍,pH<4
(3)一定温度下,将a mol/L的氨水与b mol/LH2SO4溶液等体积混合,充分反应后有:2c(SO42-)=c(NH4+),用含a和b的代数式表示该混合溶液中NH3•H2O的电离常数为$\frac{2b}{a-2b}$×10-7.
(4)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体,写出该反应的离子方程式:2Co2++N2H4+4OH-=2Co↓+N2↑+4H2O.
(5)X、Y、Z、W分别是HNO3、NH4NO3、NaOH、NaNO2四种强电解质中的一种.下表是常温下浓度均为0.01mol•L-1的X、Y、Z、W溶液的pH.
| 0.01mol•L-1的溶液 | X | Y | Z | W |
| pH | 12 | 2 | 8.5 | 4.5 |
18.下列关于硅及其化合物的叙述中,不正确的是( )
| A. | 晶体硅常用作半导体材料 | B. | 二氧化硅不能与任何酸反应 | ||
| C. | 硅在地壳中主要以化合态形式存在 | D. | 硅酸可通过硅酸钠与盐酸反应制得 |
5.如图为铜锌原电池示意图,下列说法正确的是( )


| A. | 负极发生氧化反应 | B. | 烧杯中的溶液变为蓝色 | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 该装置能将电能转变为化学能 |
15.下列关于铝及其化合物的叙述正确的是( )
| A. | Al是地壳中含量最多的元素 | |
| B. | Al2O3的熔点很高,是一种较好的耐火材料 | |
| C. | 向Al2(SO4)3溶液中滴加过量NaOH溶液制备Al(OH3) | |
| D. | 铝制品在生活中被广泛使用,说明铝是一种不活泼的金属 |
2.利用金属的活泼性不同,冶炼铝、铁、银分别应采用的方法是( )
| A. | 电解法、热还原法、热分解法 | B. | 热还原法、热分解法、电解法 | ||
| C. | 热分解法、热还原法、电解法 | D. | 电解法、热分解法、热还原法 |
19.下列说法不正确的是( )
| A. | 比较去锈的铁钉和去锈的绕有细铜丝的铁钉与同浓度的盐酸反应速率快慢时,可以加K3[Fe(CN)6]溶液,观察铁钉周围出现蓝色沉淀的快慢 | |
| B. | 将在空气中灼烧呈黑色的铜丝趁热插入盛有乙醇的试管中,铜丝变红色;反复数次,试管中的液体出现刺激性气味,表明乙醇已被铜氧化为乙醛 | |
| C. | 欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)为:中和滴定实验、pH试纸 | |
| D. | 从海带中提取碘,可将灰化后的海带加入水中煮沸一段时间后过滤,向滤液中滴入几滴硫酸,再加入适量H2O2溶液氧化,最后加入CCl4萃取分离 |
20.下列分散系中,分散质粒子的直径大小在1~100nm之间的是( )
| A. | CuSO4溶液 | B. | Fe(OH)3胶体 | C. | 稀硫酸 | D. | 浑浊的石灰水 |