题目内容
19.“南孚”牌镍氢充电电池的某极是储氢合金X(合金X结合氢气的形式表示为XH6),另一电极为NiOOH/Ni(OH)2,电解质为强碱溶液,其总反应式为:XH6+6NiOOH$?_{充电}^{放电}$X+6Ni(OH)2.下列说法正确的是( )| A. | 充电时电源的正极应与电池的X极相连 | |
| B. | 放电时负极电极反应式为:XH6+6e-═X+6H+ | |
| C. | 充电时阳极电极反应式为:6Ni(OH)2+6OH-═6NiOOH+6H2O+6e- | |
| D. | 该电池放电反应1 mol XH6时,若用于电解水,理论上可得到16g氧气 |
分析 A、充电时,电源的正极与电池的正极相连,据此回答判断;
B、放电时,原电池的负极发生失电子的氧化反应,据此书写电极反应式;
C、充电时,电解池的阳极发生失电子的氧化反应,据此书写电极反应式;
D、根据电子守恒结合化学方程式进行计算即可.
解答 解:A、总反应式为:XH6+6NiOOHXH6+6NiOOH$?_{充电}^{放电}$X+6Ni(OH)2,储氢合金X为正极,NiOOH/Ni(OH)2为负极,则充电时,电源的正极与电池的正极X相连,故A正确;
B、放电时,原电池的负极Ni(OH)2发生失电子的氧化反应,故B错误;
C、充电时,电解池的阳极发生失电子的氧化反应,即6Ni(OH)2+6OH--6e-═6NiOOH+6H2O,故C正确;
D、电池放电时反应了1molXH6,则转移电子是6mol,电解水化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,根据电子守恒,转移6mol电子时,生成氧气的物质的量是$\frac{3}{2}$×32g/mol=48g,故D错误.
故选AC.
点评 本题考查学生二次电池的工作原理以及电解池和原电池的有关知识,要求学生具有分析和解决问题的能力,难度不大.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
2.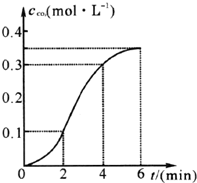 CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )
 CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )| A. | 反应开始2分钟内平均反应速率最大 | |
| B. | 反应4分钟后平均反应速率最小 | |
| C. | 反应开始4分钟内温度对反应速率的影响比浓度大 | |
| D. | 反应在第2分钟初至第3分钟末生成CO2的平均反应速率为0.1 mol/(L•min) |
10.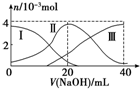 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化情况如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).根据图示判断,当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化情况如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).根据图示判断,当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序正确的是( )
 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化情况如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).根据图示判断,当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化情况如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).根据图示判断,当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序正确的是( )| A. | c(Na+)>c(HA-)>c(OH-)>c(H2A)>c(H+)>c(A2-) | B. | c(Na+)>c(HA-)>c(H+)>c(A2-)>c(H2A)>c(OH-) | ||
| C. | c(Na+)>c(H+)>c(HA-)>c(A2-)>c(OH-)>c(H2A) | D. | c(Na+)>c(OH-)>c(HA-)>c(H2A)>c(H+)>c(A2-) |
4.下列化学用语的表述不正确的是( )
| A. | 过氧化氢的结构式:H-O-O-H | B. | 氮原子的L层电子轨道表示式: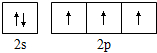 | ||
| C. | CO2的比例模型: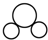 | D. | Cl-的结构示意图: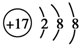 |
11.根据科学人员探测:在海洋深处的沉积物中含有可燃冰,主要成分是甲烷水合物.其组成的两种分子的下列说法正确的是( )
| A. | 它们都是极性键形成的极性分子 | |
| B. | 它们的成键方式都只有σ键 | |
| C. | 可燃冰的存在说明甲烷和水分子间能形成氢键 | |
| D. | 它们的分子空间构型都相同 |
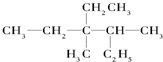 用系统命名法命名:3,4-二甲基-3-乙基己烷
用系统命名法命名:3,4-二甲基-3-乙基己烷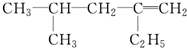
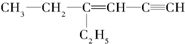 ,分子中饱和碳原子数为4个,可能在同一平面上的碳原子数最多为8个
,分子中饱和碳原子数为4个,可能在同一平面上的碳原子数最多为8个
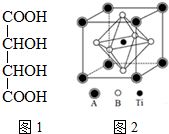 钛的化合物如TiSe2、Ti(NO3)4、TiCl4、酒石酸钛等均有着广泛用途.
钛的化合物如TiSe2、Ti(NO3)4、TiCl4、酒石酸钛等均有着广泛用途.