题目内容
A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期中原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。
请回答下列问题。
(1)元素D在周期表中的位置________。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)________________。
(3)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X,X中所含化学键类型有________。
(4)①若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:________________________________________________________________________。
②若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:________________________________________________________________。
③FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的化学方程式________________________________________________________________________。
(1)第三周期 ⅠA族 (2)S2->O2->Na+
(3)离子键、共价键、配位键(配位键不写不扣分)
(4)①2Al+Fe2O3 Al2O3+2Fe ②SiO2+2OH-=SiO32-+H2O ③2SO2+O2+2H2O=2H2SO4
Al2O3+2Fe ②SiO2+2OH-=SiO32-+H2O ③2SO2+O2+2H2O=2H2SO4
解析试题分析:原子最外层电子数是次外层电子数三倍的元素为氧元素,即C为O,则F为S;D与F同周期且其在该周期中原子半径最大,则D为Na,A为H;B的原子序数比A大比C小,其单质为气体,则B为N;E的原子序数间于Na和S之间,可能为Mg、Al、Si、P。(1)D为Na,则其在元素周期表中的位置为:第3周期I A族。(2)C、D、F三种元素形成的简单离子为:O2–、Na+、S2–,O2–与Na+具有相同的电子层结构,Na+核电荷数比O2–大,所以Na+半径比O2–小,而S2–、O2–同主族,S2–核外三层电子,O2–核外两电子,所以S2–半径比O2–大,故离子半径大小顺序为:S2–>O2–>Na+。(3)A、B、C三种元素以原子个数比4∶2∶3形成化合物为NH4NO3,NH4NO3中的化学键为离子键和共价键。(4)①若E是金属元素,其单质又能与氧化铁反应常用于焊接钢轨,则E为Al,反应的化学方程式:2Al+Fe2O3 Al2O3+2Fe;②若E是非金属元素,其单质在电子工业中有重要应用,则E可为Si,其氧化物溶于强碱溶液的离子方程式:SiO2+2OH-=SiO32-+H2O;③FC2气体有毒,排放到大气中易形成酸雨,则FC2为SO2,SO2与氧气和水蒸气反应的化学方程式为:2SO2+O2+2H2O=2H2SO4。
Al2O3+2Fe;②若E是非金属元素,其单质在电子工业中有重要应用,则E可为Si,其氧化物溶于强碱溶液的离子方程式:SiO2+2OH-=SiO32-+H2O;③FC2气体有毒,排放到大气中易形成酸雨,则FC2为SO2,SO2与氧气和水蒸气反应的化学方程式为:2SO2+O2+2H2O=2H2SO4。
考点:元素周期律、元素周期表中元素位置的确定、化学键、化学方程式书写等内容。
考点:考查

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
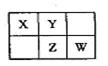
小博士期末闯关100分系列答案X、Y、Z、W、R是元素周期表前四周期中的常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | 组成蛋白质的基础元素,其最高正化合价与最低负化合价的代数和为2 |
| Y | 地壳中含量最高的元素 |
| Z | 存在质量数为23,中子数为11的核素 |
| W | 生活中大量使用其合金制品,工业上可用电解熔融氧化物的方法制备其单质 |
| R | 有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)W在元素周期表中的位置为 ;X、Y、Z、W四种元素的原子半径从大到小的顺序是 (用元素符号表示)。
(2)X与氢两元素按原子数目比1∶3和2∶4构成分子A和B,A的结构式为 ;B的电子式为 。化合物ZY中存在的化学键类型为 。
(3)砷(As)是人体必需的微量元素,与X同一主族,As原子比X原子多两个电子层,则砷的原子序数为 ,其最高价氧化物对应的水化物的化学式为 。该族二、三、四周期元素的气态氢化物的稳定性从大到小的顺序是 (用化学式表示)。
(4)用RCl3溶液腐蚀铜线路板的离子方程式为 。检验溶液中R3+常用的试剂是 ,可以观察到的现象是 。
(5)Z
 W合金(Z17W12)是一种潜在的贮氢材料,由Z、W单质在一定条件下熔炼而成。该合金在一定条件下完全吸氢的反应方程式为:Z17W12+17H2
W合金(Z17W12)是一种潜在的贮氢材料,由Z、W单质在一定条件下熔炼而成。该合金在一定条件下完全吸氢的反应方程式为:Z17W12+17H2 17ZH2+12W,得到的混合物Q(17ZH2+12W)在6.0 mol·L-1 HCl溶液中能完全释放出H2。1 mol Z17W12完全吸氢后得到的混合物Q与上述盐酸完全反应,释放出H2的物质的量为 。
17ZH2+12W,得到的混合物Q(17ZH2+12W)在6.0 mol·L-1 HCl溶液中能完全释放出H2。1 mol Z17W12完全吸氢后得到的混合物Q与上述盐酸完全反应,释放出H2的物质的量为 。 A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
| 元素 | 相关信息 |
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为3s23p1 |
| F | 基态原子的最外层p轨道有两个电子的自旋方向与其它电子的自旋方向相反 |
| G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
| H | 是我国使用最早的合金中的最主要元素 |
请用化学用语填空:
(1)A元素位于元素周期表第 周期 族,B元素和C元素的第一电离能比较,较大的是 ,C元素和F元素的电负性比较,较小的是 。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为 ,
B元素所形成的单质分子中σ键与π键数目之比为 。
(3)G元素的低价阳离子的离子结构示意图是_____________,F元素原子的价电子构型的电子排布图(轨道表示式)是__________________,H元素的基态原子核外电子排布式是 。
(4)G的高价阳离子的溶液与H单质反应的离子方程式为 ;
与E元素成对角关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的化学方程式为 。
(1)某短周期主族元素的原子M层上有一个半充满的亚层,这种原子的质子数是 ___________,写出它的外围电子排布图___________。
(2)VIA族的.硒(Se).在化合物中常表现出多种氧化态, H2SeO4比H2SeO3酸性_-___( 填强或弱),H2Se的酸性比H2S__________(填“强”或“弱”)。
(3)固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,则下列有关说法中正确的是 ( )
| A.NH5中既有离子键又有共价键 |
| B.NH5的熔、沸点高于NH3 |
| C.NH5固体投入少量水中,可产生两种气体 |
| D.0.1 mol NH5中含有5 mol N—H键 |
A、B、C、D、E、F周表前四周期中的常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| A | A是周期表中原子半径最小的元素 |
| B | B元素的原子价电子排布为ns11np14 |
| C | M的基态原子L层电子数是K层电子数的3倍 |
| D | D是第三周期中第一电离能最小的元素 |
| E | E是地壳中含量最多的金属元素 |
| F | 有多种化合价,其某种高价阳离子的价电子具有较稳定的半充满结构 |
(1)F位于元素周期表中位置 ,其基态原子核外价电子排布式为 ;
(2)B的电负性比M的 (填“大”或“小”);B2A3分子中
 键与
键与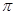 键与个数之比为 ;
键与个数之比为 ;(3)写出E的单质与D的最高价氧化物的水化物溶液反应的化学方程式: ;
(4)已知每5.4gE可与最低价F的氧化物反应,放出346.2kJ的热量。则请写出该反应的热化学方程式: 。