题目内容
20.根据如表实验操作及现象,能得到相应结论的是( )| 序号 | 操作及现象 | 结论 |
| A | 将pH为11的氨水稀释10倍,测量所得pH大于10 | 加水稀释NH3•H2O的电离程度减小 |
| B | 常温下,测得饱和Na2CO3溶液的pH大于饱和NaHCO3溶液 | 水解程度:CO32->HCO3- |
| C | 镁粉加入NH4Cl溶液中,有刺激性气味气体放出 | 该气体含有NH3 |
| D | 某气体能使酸性KMnO4溶液褪色 | 该气体一定是SO2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.NH3•H2O为弱电解质,加水稀释促进电离;
B.Na2CO3溶解度较大,应比较相同的浓度的溶液的pH;
C.镁能与氢离子反应;
D.能使酸性KMnO4溶液褪色说明有还原性.
解答 解:A.NH3•H2O为弱电解质,加水稀释促进电离,稀释10倍,测量所得pH大于10,故A错误;
B.饱和溶液的浓度不同,Na2CO3溶解度较大,应比较相同的浓度的溶液的pH,故B错误;
C.镁能与氢离子反应,促进铵根的水解,铵根水解生成氨气,故C正确;
D.能使酸性KMnO4溶液褪色说明有还原性,但是不一定是二氧化硫,也可以是硫化氢和乙醇等,故D错误.
故选C.
点评 本题考查较为综合,涉及弱电解质、盐类水解等知识,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意相关基本实验操作的注意事项,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
10.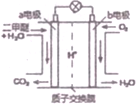 二甲醚是一种绿色、可再生的新能源,如图是绿色电源“燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法错误的是( )
二甲醚是一种绿色、可再生的新能源,如图是绿色电源“燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法错误的是( )
 二甲醚是一种绿色、可再生的新能源,如图是绿色电源“燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法错误的是( )
二甲醚是一种绿色、可再生的新能源,如图是绿色电源“燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法错误的是( )| A. | a电极为该电池负极 | |
| B. | O2在b电极上得电子,被氧化 | |
| C. | 电池工作时,燃料电池内部H+从a电极移向b电极 | |
| D. | 电池工作时,a电极反应式:CH3OCH3-12e-+3H2O═2CO2↑+12H+ |
8.已知反应NO2(g)+CO(g)═NO(g)+CO2(g)的能量变化如图所示,下列说法正确的是( )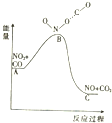

| A. | 该反应为放热反应 | |
| B. | 该反应为非氧化还原反应 | |
| C. | 1molNO2和1molCO的键能总和大于1molNO和1molCO2的键能总和 | |
| D. | 1molNO2(g)和1molCO(g)的总能量低于1mol NO(g)和1molCO2(g)的总能量 |
15. A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.
A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.
(1)将A、E两种元素的元素符号填入下表中正确的位置上.
(2)A、B、C、D、E、F六种元素中非金属性最强的是F(填元素符号),B、D量元素可以组成原子个数比为1:1的离子化合物,写出该离子化合物的电子式: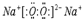 ,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).
,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).
(3)写出D、F两元素的最高价氧化物对应的水化物反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
 A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.
A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.(1)将A、E两种元素的元素符号填入下表中正确的位置上.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 一 | ----------------- | |||||||
| 二 | ||||||||
| 三 | ||||||||
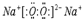 ,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).
,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).(3)写出D、F两元素的最高价氧化物对应的水化物反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
5.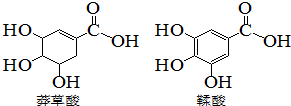 莽草酸是一种合成治疗甲型H7N9流感药物达菲的原料,鞣酸存在与苹果、生石榴等植物中,下列关于这两种有机化合物的说法错误的是( )
莽草酸是一种合成治疗甲型H7N9流感药物达菲的原料,鞣酸存在与苹果、生石榴等植物中,下列关于这两种有机化合物的说法错误的是( )
 莽草酸是一种合成治疗甲型H7N9流感药物达菲的原料,鞣酸存在与苹果、生石榴等植物中,下列关于这两种有机化合物的说法错误的是( )
莽草酸是一种合成治疗甲型H7N9流感药物达菲的原料,鞣酸存在与苹果、生石榴等植物中,下列关于这两种有机化合物的说法错误的是( )| A. | 可用浓溴水区分两种酸 | |
| B. | 可用红外光谱区分两种酸 | |
| C. | 等物质的量的两种酸,分别于足量钠反应,生成氢气的质量相等 | |
| D. | 两种酸分子中所以碳原子均在同一平面上 |
12.如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )


| A. | 石墨和金刚石的转化是物理变化 | |
| B. | 金刚石的稳定性强于石墨 | |
| C. | 1 mol石墨的总键能比1 mol金刚石的总键能大 1.9 kJ | |
| D. | C(s,石墨)=C(s,金刚石),该反应的焓变(△H)为负值 |
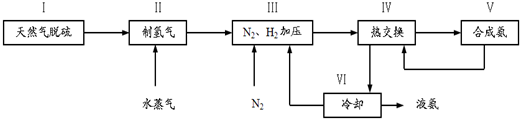
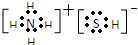 ,写出再生反应的化学方程式:2NH4HS+O2=2S↓+2NH3•H2O.NH3的沸点高于H2S,是因为NH3分子之间存在着一种比分子间作用力更强的作用力.
,写出再生反应的化学方程式:2NH4HS+O2=2S↓+2NH3•H2O.NH3的沸点高于H2S,是因为NH3分子之间存在着一种比分子间作用力更强的作用力.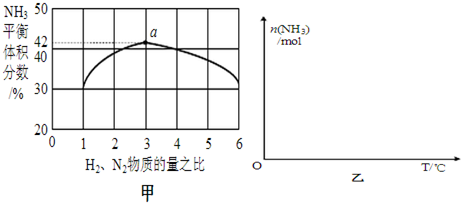
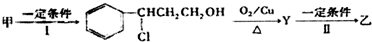
 +HCl$\stackrel{一定条件下}{→}$
+HCl$\stackrel{一定条件下}{→}$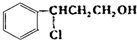 ,反应II的反应类型为消去反应.
,反应II的反应类型为消去反应. .
.